
科目:高中化学 来源: 题型:解答题
 利用氮气、氢气在一定条件下生成氨气这一可逆反应来合成氨,是一个重要的化工反应.常用来生产液氨和氨水.
利用氮气、氢气在一定条件下生成氨气这一可逆反应来合成氨,是一个重要的化工反应.常用来生产液氨和氨水.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 溶质 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
| A. | 0.1 mol•L-1 Na2CO3溶液中,存在关系:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) | |
| B. | 加热0.1 mol•L-1 NaClO溶液测其pH,pH小于9.7 | |
| C. | pH=2的HF溶液与pH=12的NaOH溶液以等体积混合,则有c(Na+)=c(F-)>c(H+)=c(OH-) | |
| D. | 根据上表数据得出三种酸电离平衡常数大小关系为:HF>HClO>H2CO3(一级电离平衡常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L H2 与O2的混合气体所含原子数为2NA | |
| B. | 标准状况下,18g H2O的体积是22.4L | |
| C. | NA个SO2的体积是22.4L | |
| D. | 在常温、常压下,11.2L N2含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现有含有少量KCl、K2SO4、K2CO3杂质的KNO3溶液,选择适当的试剂除去杂质,得到纯净的KNO3固体,实验流程如图所示.
现有含有少量KCl、K2SO4、K2CO3杂质的KNO3溶液,选择适当的试剂除去杂质,得到纯净的KNO3固体,实验流程如图所示.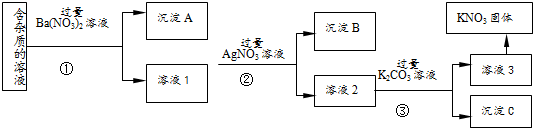
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaOH溶液中逐滴滴入饱和氯化铁溶液来制备Fe(OH)3胶体 | |
| B. | 向Fe(OH)3胶体中逐滴滴入稀盐酸,现象是先出现红褐色沉淀,后溶解转为黄色溶液 | |
| C. | “丁达尔”效应是区分胶体和溶液的唯一手段 | |
| D. | 静电除尘与胶体性质无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

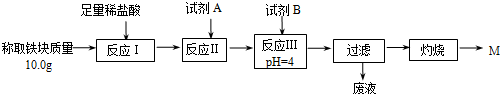
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
| 操作 | 预期现象 |
| 取少量M固体于试管中,向其中加入足量稀硫酸;观察. | 固体完全溶解,溶液呈黄色. |
继续向上述溶液中滴入几滴(少量)高锰酸钾溶液,振荡观察 | 溶液紫红色未褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述三个反应都有单质生产,所以都是置换反应 | |
| B. | 氧化性由强到弱的顺序为KBrO3>KClO3>Cl2>Br2 | |
| C. | 反应①中还原剂与氧化剂的物质的量之比为6:1 | |
| D. | 若反应②中有1 mol还原剂参加反应,则氧化剂得电子的物质的量为2mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com