
| 实验编号 | 操 作 | 现 象 |
I |
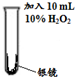 |
剧烈反应,有大量无色气体产生,该气体可以使带火星的木条复燃;反应停止后,试管内壁上的银全部溶解,得到澄清液体a. |
| 实验编号 | 操 作 | 现 象 |
Ⅱ |
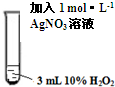 |
振荡,溶液无明显现象. |
Ⅲ |
 |
剧烈反应,产生大量无色气体,同时在试管底部仍有少量黑色固体. |
| 实验步骤和操作 | 实验现象及结论 |
| 取3mL 10% H2O2在试管中,加入少量Ag2O,充分反应后, |


科目:高中化学 来源: 题型:
| A、食盐水放在试管中进行蒸发可得到NaCl固体 |
| B、过滤操作中,使用玻璃仪器有烧杯、漏斗、玻璃棒 |
| C、分液漏斗能用于混合物混合物的分离和组装滴加液体制气体的发生装置 |
| D、可用量筒快速配制一定体积、一定物质的量浓度的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
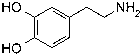 爱情是什么?化学家通过研究发现:大脑中心贮藏一种恋爱兴奋剂----多巴胺.当一对男女一见钟情或产生爱慕之情时,多巴胺就源源不断地分泌出来,于是爱情势不可挡地汹涌而出.多巴胺结构如图:
爱情是什么?化学家通过研究发现:大脑中心贮藏一种恋爱兴奋剂----多巴胺.当一对男女一见钟情或产生爱慕之情时,多巴胺就源源不断地分泌出来,于是爱情势不可挡地汹涌而出.多巴胺结构如图: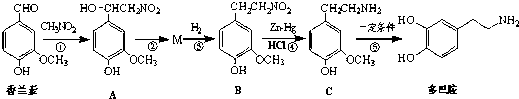
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用.
氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸馏法将海水淡化为饮用水 |
| B、三氯化铁溶液滴入沸水中制胶体 |
| C、渗析法除去淀粉溶胶中的NaCl |
| D、向Fe(OH)3胶体中加入MgSO4溶液产生沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com