
 2SO3(g)+196.6 kJ,下列说法正确的是
2SO3(g)+196.6 kJ,下列说法正确的是| A.1 molSO2(g)的能量总和大于lmol S(s)和l molO2(g)的能量总和 |
| B.将2 molSO2(g)与l molO2(g)在一定条件下充分反应,放出196.6kJ的热量 |
C.S(g)+O2(g) SO2(g)+Q,Q值小于297.16 kJ SO2(g)+Q,Q值小于297.16 kJ |
| D.当l mol S(s)完全转化为SO3(g)时(假设无热量损失),放出395.46kJ的热量 |
 2SO3(g) 是可逆反应,反应物的转化率得不到100%,因此将2 molSO2(g)与l molO2(g)在一定条件下充分反应,放出的热量小于196.6kJ,B不正确;C、气态S的能量高于固态S的能量,所以气态S燃烧放出的热量多,即S(g)+O2(g)→SO2(g)+Q,Q值大于297.16 kJ,C不正确;D、根据盖斯定律可知,S(s)+
2SO3(g) 是可逆反应,反应物的转化率得不到100%,因此将2 molSO2(g)与l molO2(g)在一定条件下充分反应,放出的热量小于196.6kJ,B不正确;C、气态S的能量高于固态S的能量,所以气态S燃烧放出的热量多,即S(g)+O2(g)→SO2(g)+Q,Q值大于297.16 kJ,C不正确;D、根据盖斯定律可知,S(s)+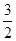 O2(g)→SO3(g),所以该反应放出的热量是297.16kJ+
O2(g)→SO3(g),所以该反应放出的热量是297.16kJ+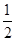 ×196.6 kJ=395.46kJ,D正确,答案选D。
×196.6 kJ=395.46kJ,D正确,答案选D。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源:不详 题型:填空题
 3N2+2X+4H2O
3N2+2X+4H2O 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 .
. 、一283.0 kJ
、一283.0 kJ 和一726.5.kJ
和一726.5.kJ 。请回答下列问题:
。请回答下列问题: 、
、 均大于300℃):
均大于300℃):
 时,从反应开始到反应达到平衡,生成甲醇的平均速率为:
时,从反应开始到反应达到平衡,生成甲醇的平均速率为:
 时的平衡常数比
时的平衡常数比 时的小
时的小 变到
变到 ,达到平衡时
,达到平衡时 增大
增大 温度时,将1mol CO2和3mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为a,则此时容器内的压强与起始压强之比为___________。
温度时,将1mol CO2和3mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为a,则此时容器内的压强与起始压强之比为___________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 4NO(g)+6H2O(g) △H =" —905" kJ/mol ①主反应
4NO(g)+6H2O(g) △H =" —905" kJ/mol ①主反应 2N2(g)+6H2O(g) △H =" —1268" kJ/mol ②副反应
2N2(g)+6H2O(g) △H =" —1268" kJ/mol ②副反应
 2NO(g)的反应热ΔH=
2NO(g)的反应热ΔH= 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
 N2+2CO2 ΔH<0研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反 应速率的影响规律、某同学设计了三组实验,部分实验条件已经填在下表中。
N2+2CO2 ΔH<0研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反 应速率的影响规律、某同学设计了三组实验,部分实验条件已经填在下表中。

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.330 kJ | B.276.67 kJ | C.130 kJ | D.76.67 kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.在100 ℃.101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g) H2O(l) 的ΔH ="+" 40.69 kJ·mol-1 H2O(l) 的ΔH ="+" 40.69 kJ·mol-1 |
| B.已知MgCO3的Ksp = 6.82 × 10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+) = c(CO32-),且c(Mg2+) · c(CO32-)= 6.82 × 10-6 |
| C.常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的pH减小 |
| D.已知: |
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
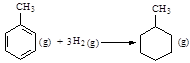 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3(g) △H="-Q" kJ·mol-1(Q>0),测得SO2的转化率为90%,
2SO3(g) △H="-Q" kJ·mol-1(Q>0),测得SO2的转化率为90%,| A.1.8Q kJ | B.2Q kJ | C.Q kJ | D.0.9 QJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com