
| A. | 电子由电极Ⅳ通过外电路流向电极Ⅰ | |
| B. | 装置工作过程中Ⅲ电极周围出现红色 | |
| C. | 电极Ⅱ发生还原反应 | |
| D. | 盐桥中Cl-向乙池移动 |
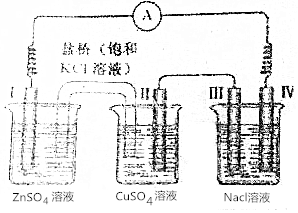
分析 I是锌、其余电极都是石墨,锌易失电子作负极,II是正极,甲、乙构成原电池,丙有外接电源,属于电解池,III为阳极、IV为阴极,
A.电子从负极沿导线流向阴极;
B.III电极是阳极,阳极上氯离子放电生成氯气;
C.电极II上铜离子得电子析出Cu单质;
D.盐桥中氯离子向负极区域移动.
解答 解:I是锌、其余电极都是石墨,锌易失电子作负极,II是正极,甲、乙构成原电池,丙有外接电源,属于电解池,III为阳极、IV为阴极,
A.电子从负极I沿导线流向阴极IV,故A错误;
B.III电极是阳极,阳极上氯离子放电生成氯气,IV为阴极,阴极上氢离子放电生成氢气,同时电极附近生成氢氧根离子,导致溶液变红色,故B错误;
C.电极II上铜离子得电子发生还原反应而析出Cu单质,故C正确;
D.盐桥中氯离子向负极甲池区域移动,故D错误;
故选C.
点评 本题考查探究原电池原理,侧重考查分析能力,明确各个电极上发生的反应是解本题关键,知道哪些装置构成原电池、哪些装置构成电解池,易错选项是D,注意盐桥中阴阳离子移动方向.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA | |
| B. | 标准状况下,2.24 LCCl4含有的共价键数为0.4NA | |
| C. | 1 L 0.1 mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1 NA | |
| D. | 14 g乙烯和丙烯混合气体中的氢原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCH3+所含的电子数为9NA | |
| B. | 标准状况下,11.2 L HF的分子数为0.5NA | |
| C. | 39 g Na2O2与足量水反应,转移电子数为NA | |
| D. | 1 mol乙醇中含有共用电子对数为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯分子可表示为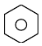 ,其邻二氯代物有2种结构 ,其邻二氯代物有2种结构 | |
| B. | 等物质的量C2H4、C3H6完全燃烧,消耗等质量的O2 | |
| C. | 蛋白质的水解和油脂的皂化都是由高分子生成小分子的过程 | |
| D. | 利用CH4和Cl2的取代反应可制取溶剂CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
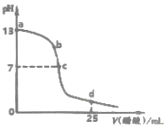 如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )
如图为常温下0.2000mol•L-1 CH3COOH溶液逐滴加入到25mL0.1000mol•L-1 NaOH溶液中pH的变化曲线,下列说法不正确的是( )| A. | a~c区间内(不包含a、c两点)可能存在:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| B. | c点时溶液中:c(Na+)=c(CH3COO-) | |
| C. | d点时溶液中:c(Na+)+c(H+)+c(CH3COOH)-c(OH-)=0.2000mol•L-1 | |
| D. | 反应过程中溶液中阴、阳离子总数:b点小于c点 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com