
【题目】有关物质的转化关系如图所示(部分生成物和反应条件已略去)。D、F、G、H均为常见气体,其中D能使湿润的红色石蕊试纸变蓝,G呈黄绿色,H在空气中含量最高;C的摩尔质量为32g·mol-1;E为难溶性碱。
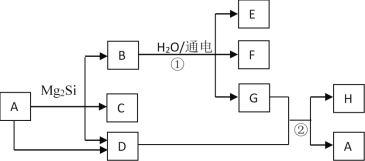
(1)C的化学式为_________;
(2)A的电子式为_________;
(3)写出反应①的离子方程式_______________;
(4)写出反应②的化学方程式________________。
【答案】SiH4 ![]() Mg2+ +2Cl-+2H2O
Mg2+ +2Cl-+2H2O![]() Mg(OH)2↓ +H2↑ +Cl2↑ 8NH3+3Cl2=6NH4Cl +N2
Mg(OH)2↓ +H2↑ +Cl2↑ 8NH3+3Cl2=6NH4Cl +N2
【解析】
D能使湿润的红色石蕊试纸变蓝,D为NH3,G呈黄绿色,G为Cl2,H在空气中含量最高,H为N2,氯气和氨气反应生成氮气和A,A在一定条件下可以转化为氨气,则A为氯化铵(NH4Cl),E为难溶性碱,由转化关系可知,E为Mg(OH)2,B应为MgCl2,则F为H2;C的摩尔质量为32gmol-1,由转化关系可知,C中含有Si元素,则C为SiH4。据此分析解答。
(1)由以上分析可知C为SiH4,故答案为:SiH4;
(2)A为NH4Cl,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)反应①为氯化镁溶液的电解,反应的离子方程式为Mg2++2Cl-+2H2O![]() H2↑+Cl2↑+Mg(OH)2↓,故答案为:Mg2++2Cl-+2H2O
H2↑+Cl2↑+Mg(OH)2↓,故答案为:Mg2++2Cl-+2H2O![]() H2↑+Cl2↑+Mg(OH)2↓;
H2↑+Cl2↑+Mg(OH)2↓;
(4)反应②为氯气和氨气的反应,反应的化学方程式为8NH3+3Cl2═N2+6NH4Cl,故答案为:8NH3+3Cl2═N2+6NH4Cl。


科目:高中化学 来源: 题型:
【题目】现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10m) | 0.74 | 1.60 | 1.86 | 1.10 | 0.99 | 1.52 | 0.75 | 1.43 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
-2 | -3 | -1 | -3 |
回答下列问题:
(1)⑥的单质在空气中加热,生成物的电子式为_______________。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是___________。
(3)比较①和⑦的氢化物的稳定性(用化学式表示)_______________________________。
(4)写出实验室制备⑤的单质的离子方程式:________________________________。
(5)写出⑧的单质跟③的最高价氧化物的水化物的溶液反应的离子方程式:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中亚硫酸表现的性质,其中一种与另外三种不同的是( )
A.能使酸性高锰酸钾褪色B.在空气中易被氧化变质
C.能使溴水褪色D.在溶液中加入氢氧化钡溶液产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸钡(BaTiO3)在工业上有重要用途,主要用于制作电子陶瓷、PTC热敏电阻、电容器等多种电子元件。以下是生产钛酸钡的一种工艺流程图:
![]()
已知:①草酸氧化钛钡晶体的化学式为BaTiO(C2O4)2·4H2O;
(1)BaTiO3中Ti元素的化合价为:__________。
(2)用盐酸酸浸时发生反应的离子方程式为: ________________________________。
(3)流程中通过过滤得到草酸氧化钛钡晶体后,为提高产品质量需对晶体洗涤。
①过滤操作中使用的玻璃仪器有__________________________________________。
②如何证明晶体已洗净?_________________________________________。
(4)某兴趣小组取19.70gBaCO3模拟上述工艺流程制备BaTiO3,得产品13.98g,BaTiO3的产率为:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种物质中均含有同一种元素,它们之间有如下图所示的转化关系(部分反应物质已略去)下列说法不正确的是
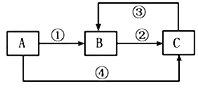
A. 若A是一种两性氧化物,则B的水溶液可呈酸性,C的水溶液可呈碱性
B. 若A是一种金属单质,则反应①②③均可为化合反应,反应④可为置换反应
C. 若A、B均是可燃性物质,完全燃烧都生成气体C,常温下A溶液PH<7,则将C通入A溶液中,pH先减小后增大
D. 若A、B、C是三种不同类别的固体物质,则B可以是工业上制取A、C的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,在固定容积的密闭容器中,能表示反应X(气)+2Y(气)![]() 2Z(气)一定达到化学平衡状态的是( )
2Z(气)一定达到化学平衡状态的是( )
A.容器内压强不随时间改变
B. c(X).c(Y)2=c(Z)2
C.正反应生成Z的速率与逆反应生成X的速率相等
D.容器内混合气体的密度不随时间改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.010 mol/L的这四种溶液pH与该元素原子半径的关系如图所示。下列说法正确的是
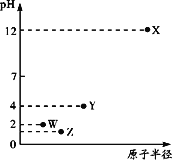
A. 简单离子半径:X>Y>Z>W
B. Y元素存在同素异形体
C. 气态氢化物的稳定性:Z>W>Y
D. X和Y的最高价氧化物对应的水化物恰好中和时,溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种固态物质熔化(或升华)时,克服的微粒间相互作用力属于同种类型的是( )
A.碘和碘化钠B.金刚石和大理石
C.冰醋酸和硫磺D.干冰和二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.在恒温、体积为1.0L的密闭容器中通入1.0molN2和xmolH2发生如下反应N2(g)+3H2(g)![]() 2NH3(g),20min后达到平衡,测得反应放出的热量为18.4kJ,混合气体的物质的量为1.6mol,容器内的压强变为原来的80%。请回答下列问题:
2NH3(g),20min后达到平衡,测得反应放出的热量为18.4kJ,混合气体的物质的量为1.6mol,容器内的压强变为原来的80%。请回答下列问题:
(1)20min内,V(N2)=______。
(2)该反应的热化学方程式为____________。
(3)下列叙述中能表示该反应达到平衡状态的是_______(填序号)。
①N2体积分数保持不变②单位时间断裂03tmolH-H键,同时生成0.6molN-H键
③混合气体的密度不再改变④2v正(H2)=3v逆(NH3)⑤混合气体的平均摩尔质量不再改变
II.1883年,瑞典化学家阿伦尼乌斯创立了电离学说,在水溶液范围内对酸、碱作出了严密的概括。请回答下列有关水溶液的问题:
(4) ①用电离方程式表示氨水溶液是碱性的原因________;
②用离子方程式表示碳酸钠溶液显碱性的原因__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com