
“金属钙线”是炼制优质钢材的脱氧脱磷剂,某“金属钙线”的主要成分为金属M和金属钙Ca,并含有3.5%(质量分数)CaO。
(1)Ca的原子结构示意图为 。其最高价氧化物对应水化物的碱性比Mg(OH)2 (填“强”或“弱”)。
(2)Ca与非金属性最强的元素A形成化合物D,用电子式表示D的形成过程: 。
(3)配平用“金属钙线”脱氧脱磷的方程式:
(4)将“金属钙线”溶于稀盐酸后,滴加少量双氧水后再滴加KSCN溶液呈红色,金属M为 (填化学式), 其中滴加双氧水发生的离子方程式是 。
(5)取3.2 g“金属钙线”试样,与水充分反应生成448 mL H2(标准状况),在所得溶液中通入适量CO2,最多能得到CaCO3 g。
(1)Ca的原子结构示意图 ; 强
; 强
(2)CaF2的形成过程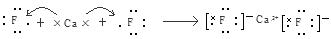 ;
;
(3)2,5,3,1,5
(4)Fe ; 2Fe2++ H2O2 + 2H+= 2Fe3+ + 2H2O
(5)2.2g ;
解析试题分析:(1)20号元素的原子核外电子排布为2、8、8、2.所以其结构示意图为 。Ca、Mg是同一主族的元素,从上到下元素的金属性逐渐增强,所以金属性:Ca>Mg。元素的金属性越强,其最高价氧化物对应的水化物的碱性越强。因此碱性Ca(OH)2>Mg(OH)2。(2)金属性很强的元素Ca与非金属性最强的元素F形成化合物CaF2是离子化合物。其形成过程用电子式表示为:
。Ca、Mg是同一主族的元素,从上到下元素的金属性逐渐增强,所以金属性:Ca>Mg。元素的金属性越强,其最高价氧化物对应的水化物的碱性越强。因此碱性Ca(OH)2>Mg(OH)2。(2)金属性很强的元素Ca与非金属性最强的元素F形成化合物CaF2是离子化合物。其形成过程用电子式表示为: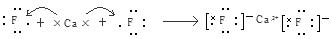 (3)在氧化还原反应中化合价升高与降低的总数相等。该反应的方程式为2P+5FeO+3CaO
(3)在氧化还原反应中化合价升高与降低的总数相等。该反应的方程式为2P+5FeO+3CaO 1Ca3(PO4)2+5Fe。(4)将“金属钙线”溶于稀盐酸后,滴加少量双氧水后再滴加KSCN溶液呈红色,金属M为Fe。 在该 中发生的反应为:FeO+2HCl= FeCl2+H2O;当向其中滴加双氧水时,发生氧化还原反应,在氧化还原反应中化合价升高与降低的总数相等。因此该反应的离子方程式是2Fe2+ + H2O2 + 2H+= 2Fe3+ + 2 H2O。(5)“金属钙线”试样,与水充分反应生成448 mL H2。因为只有Ca可以与水发生反应产生氢气:Ca+2H2O=Ca(OH)2+ H2↑。n(H2)=" 0.448L" ÷22.4L/mol="0.02mol.n(CaO)=" (3.2 g×3.5%)÷56g/mol=0.002mol.所以一共产生的Ca(OH)2的物质的量为:n(Ca(OH)2)=0.022mol.在所得溶液中通入适量CO2,发生反应:CO2+Ca(OH)2=CaCO3↓+H2O所以得到的CaCO3质量最多为0.022mol×100g/mol=2.2g。
1Ca3(PO4)2+5Fe。(4)将“金属钙线”溶于稀盐酸后,滴加少量双氧水后再滴加KSCN溶液呈红色,金属M为Fe。 在该 中发生的反应为:FeO+2HCl= FeCl2+H2O;当向其中滴加双氧水时,发生氧化还原反应,在氧化还原反应中化合价升高与降低的总数相等。因此该反应的离子方程式是2Fe2+ + H2O2 + 2H+= 2Fe3+ + 2 H2O。(5)“金属钙线”试样,与水充分反应生成448 mL H2。因为只有Ca可以与水发生反应产生氢气:Ca+2H2O=Ca(OH)2+ H2↑。n(H2)=" 0.448L" ÷22.4L/mol="0.02mol.n(CaO)=" (3.2 g×3.5%)÷56g/mol=0.002mol.所以一共产生的Ca(OH)2的物质的量为:n(Ca(OH)2)=0.022mol.在所得溶液中通入适量CO2,发生反应:CO2+Ca(OH)2=CaCO3↓+H2O所以得到的CaCO3质量最多为0.022mol×100g/mol=2.2g。
考点:考查元素的推断、原子结构示意图、离子化合物的电子式表示、元素的金属性强弱的比较、氧化还原反应方程式的配平、Fe3+离子的检验、离子方程式的书写及有关化学计算的知识。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
(12分)某研究性学习小组在网上搜集到信息:钾、钙、钠、镁等活泼金属能在CO2气体中燃烧。他们对钠在CO2气体中燃烧进行了下列实验:
| 操作过程 | 实验现象 |
| 将干燥的玻璃燃烧匙中燃烧的钠迅速 伸入到盛有装满CO2的集气瓶中 | 钠在盛有CO2的集气瓶中继续燃烧 |
| 反应后冷却 | 集气瓶底附着黑色颗粒,瓶壁上附着有白色 物质 |
| 实验步骤 | 实验现象 |
| ①取少量白色物质于试管中,加入适量水,振荡,样品全 部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
单质A与粉末化合物B组成的混合物能发生如图所示的一系列反应: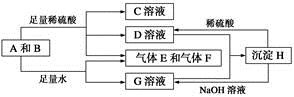
请回答下列问题:
(1)组成A单质的元素在周期表中处于第__________周期__________族。
(2)化合物B的电子式为_____________________________。
(3)D与G两溶液混合后发生反应的离子方程式为____________________
(4)常温下,D溶液的pH________7(填“>”、“<”或“=”),其原因是____________________________(用离子方程式表示)。
(5)10.8 g A单质与足量的NaOH溶液反应,消耗氧化剂的质量为________ g。
(6)用碳棒、稀硫酸、气体E和气体F组成燃料电池,该电池的正极反应式为______________________。以该电池为电源,用惰性电极电解100 g 8%的C溶液,电解到溶质的质量分数为12.5%时停止电解,则电解过程中,生成的气体在准状况下的体积共为________ L,电路上通过电子的物质的量为________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
纯碱(Na2CO3)在生产生活中具有广泛的用途。以下是实验室模拟制碱原理制取Na2CO3的流程图。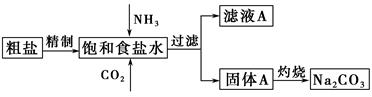
已知:向饱和食盐水中通入NH3、CO2后发生的反应为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+、Mg2+、SO42-等。
精制除杂的步骤顺序是a→ → → →b(填字母编号)。
a.粗盐溶解,滤去沉渣
b.加入盐酸调pH
c.加入Ba(OH)2溶液
d.加入Na2CO3溶液
e.过滤
向饱和食盐水中先通入NH3,后通入CO2,理由是 。
(2)灼烧固体A制Na2CO3在 (填字母序号)中进行。
a.坩埚 b.蒸发皿 c.烧杯 d.锥形瓶
证明滤液A中含有NH4+的方法是 。
对滤液A进行重结晶能够获得NH4HCO3,向pH=13含Na+、K+的溶液中加入少量NH4HCO3使pH降低,反应的离子方程式为 。
(3)下图装置中常用于实验室制备CO2的是 (填字母编号);用b装置制备NH3,分液漏斗中盛放的试剂是 (填试剂名称),烧瓶内可加入的固体试剂是 (填试剂名称)。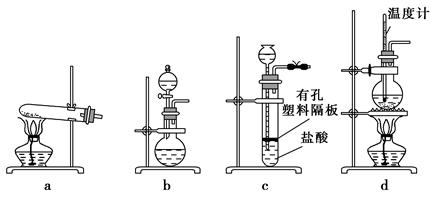
(4)一种天然碱晶体成分是aNa2CO3·bNa2SO4·cH2O,某同学利用下列提供的试剂,设计了如下简单合理测定Na2CO3的质量分数的实验方案。(仪器自选)请把实验方案填全:
供选择的试剂:1.0 mol·L-1 H2SO4溶液、1.0 mol·L-1 BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
①称取m1g天然碱晶体样品,溶于适量蒸馏水中。
② 。
③ 。
④计算天然碱晶体中含Na2CO3的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
1862年,比利时化学家索尔维发明了氨碱法制碱,1926年,我国化学家侯德榜创立了
更为进侯德榜制碱法,也叫联合制碱法,两种制碱的生产流程可简要表示如下图: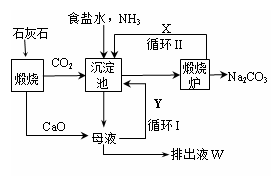

氨碱法生产流程 联合制碱法生产流程
(1)向沉淀池中通入CO2和氨气时,应先通入氨气的原因是 。
(2)沉淀池中发生反应的化学反应方程式是 从沉淀池中分离沉淀的操作是 。
(3)氨碱法生产流程示意图中的Y是 ,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为 。
(4)联合制碱法中从滤液中提取氯化铵晶体的过程推测,所得结论正确是 (选填编号)。
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气能增大NH4+的浓度,使氯化铵更多析出
c.加入食盐细粉能提高Na+的浓度, 使NaHCO3结晶析出
d.通入氨气能使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
(5)联合制碱法相比于氨碱法,氯化钠利用率从70%提高到90%以上,主要是设计了循环Ⅰ,联合制碱法的另一项优点是 。
(6)产品纯碱中含有碳酸氢钠,可以用加热分解的方法测定产品中纯碱的质量分数,已知样品质量为ag,加热至质量不再改变时称重为bg,则纯碱的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下面是有关物质的转化关系图(有些物质已省略)。
若A为单质,E在常温下为液体,C的相对分子质量为78。请回答下列问题: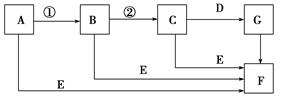
(1)画出A的原子结构示意图________,F的电子式是________。
(2)下面对C物质结构、性质的推断中,不正确的是________。
| A.久置于空气中会变成白色 |
| B.具有强氧化性 |
| C.晶体中存在离子键和共价键 |
| D.遇湿润的紫色石蕊试纸只能使其变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
LiBH4为近年来储氢材料领域的研究热点。
(1)反应2LiBH4=2LiH+2B+3H2↑,生成22.4 L H2(标准状况)时,转移电子的物质的量为 mol。
(2)下图是2LiBH4/MgH2体系放氢焓变示意图,则:
Mg(s)+2B(s)=MgB2(s) △H= 。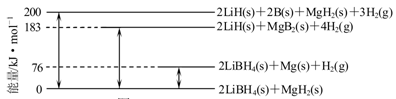
(3)采用球磨法制备Al与LiBH4的复合材料,并对Al-LiBH4体系与水反应产氢的特性进行下列研究:
①如图为25℃水浴时每克不同配比的Al-LiBH4复合材料与水反应产生H2体积随时间变化关系图。由图可知,下列说法正确的是 (填字母)。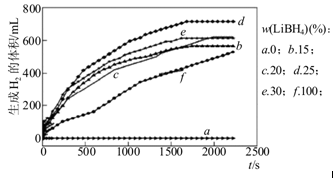
a.25℃时,纯铝与水不反应
b.25℃时,纯LiBH4与水反应产生氢气
c.25℃时,Al-LiBH4复合材料中LiBH4含量越高,1000s内产生氢气的体积越大
②如图为25℃和75℃时,Al-LiBH4复合材料[ω(LiBH4)=25%]与水反应一定时间后产物的X-射线衍射图谱(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。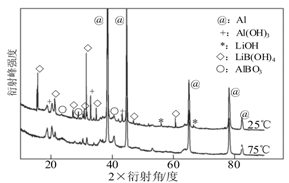
从图中分析,25℃时Al-LiBH4复合材料中与水完全反应的物质是 (填化学式),产生Al(OH)3的化学方程式为 。
(4)如图是直接硼氢化钠-过氧化氢燃料电池示意图。该电池工作时,正极附近溶液的pH (填“增大”、“减小”或“不变”),负极的电极反应式为 。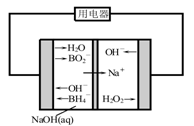
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)要确定铁的某氯化物FeClx的化学式,可用离子交换和滴定的方法。实验中称取0.54 g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40 mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0 mL。计算该样品中氯的物质的量,并求出FeClx中x值:______________________________________ (列出计算过程);
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为________。在实验室中,FeCl2可用铁粉和________反应制备,FeCl3可用铁粉和________反应制备;
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为________________;
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为_____________________________。与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为______________________,该电池总反应的离子方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示:
根据上述图示,完成下列填空:
(1)明矾石焙烧后用稀氨水浸出。配制500mL稀氨水(每升含有39.20g氨)需要取浓氨水(每升含有251.28g氨)__________mL,用规格为_______mL量筒量取。
(2)氨水浸出后得到固体混合体系,过滤,滤液中除K+、SO42-外,还有大量的NH4+。检验NH4+的方法是______________________________________________。
(3)写出沉淀物中所有物质的化学式________________________________________。
(4)滤液I的成分是水和______________。
(5)为测定混合肥料K2SO4、(NH4)2SO4中钾的含量,请完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量______溶液,产生白色沉淀。
②___________、__________、_________(依次填写实验操作名称)。
③冷却、称重。
(6)若试样为mg,沉淀的物质的量为nmol,则试样中K2SO4的物质的量为:___________mol(用含有m、n的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com