
芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。
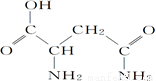
(1)天冬酰胺所含元素中,________(填元素名称,下同)元素基态原子核外未成对电子数最多,第一电离能最大的是________。
(2)天冬酰胺中碳原子的杂化轨道类型为________,分子中σ键和π键数目之比为________。
(3)O、S、Se为同主族元素,H2O、H2S和H2Se的参数对比见表。
化学式 | 键长/nm | 键角 |
H2O | 0.99 | 104.5° |
H2S | 1.34 | 92.3° |
H2Se | 1.47 | 91.0° |
H2S的键角大于H2Se的原因可能为________________________________________。
H2O、H2S、H2Se沸点由高到低的顺序为________________,酸性由强到弱的顺序为________________。
(4)写出铬的基态原子电子排布式:________________________________________。
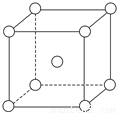
(5)铬为体心立方晶体,晶胞结构如图,则该晶胞中含有______个铬原子。若铬的密度为ρg·cm-3,相对原子质量为M,NA表示阿伏加德罗常数的值,则铬原子的半径为______cm。
科目:高中化学 来源:2017届江西省南昌市高三第一次模拟考试理综化学试卷(解析版) 题型:简答题
水合碱式碳酸镁[4MgC03·Mg(OH)2·4H2O〕,又称轻质碳酸镁。常利用菱镁矿(质量含量为碳酸镁90% ,碳酸钙10%〕碳化法制取:

(1)根据下列表格数据,选择消化反应的最佳温度_____;理由是__________。

(2)碳化反应可生成Mg(HCO3)2,生成Mg(HCO3)2的化学方程式为_______。
(3)流程图中______和_____可以为碳化反应提供二氧化碳源。
(4)有工艺设计利用卤水碳化法制取轻质碳酸镁:
①卤水中含有Fe2+和Mn2+,当其浓度小于1×10-5时,可以认为完全除去。常温时当调节溶液pH为9.5时,此时Mn2+小于_____mol/L,不会沉淀出来。

②如果把Fe2+转化为Fe3+,从环境角度选择最合适的氧化剂为______。
A. Ca(C10)2 B. Cl2 C. H202 D. HNO3
③下列方案中,较好的为_______,理由是___________。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列实验现象与氧化还原反应有关的是
A. 向碳酸钠溶液中滴加氯化钙溶液,产生白色沉淀
B. 向含有酚酞的氢氧化钠溶液中滴加盐酸,红色褪去
C. 向硅酸钠溶液中通入二氧化碳,产生白色胶状沉淀
D. 硫酸铜溶液中插入铁片,铁片上出现红色物质
查看答案和解析>>
科目:高中化学 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
一定温度下,体积不变的密闭容器中,对可逆反应A(g) + 2B(g)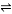 3C(g) + D(s) 的下列叙述中,能说明反应已达到平衡的是:
3C(g) + D(s) 的下列叙述中,能说明反应已达到平衡的是:
A. 单位时间内消耗a mol A,同时生成3a mol C
B. C的生成速率与C的分解速率相等
C. 混合气体的总物质的量不再变化
D. 容器内的压强不再变化
查看答案和解析>>
科目:高中化学 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:选择题
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是:
X | Y | Z | |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液 | SiO2 | 浓盐酸 |
③ | FeCl3溶液 | Cu | 浓硝酸 |
④ | O2 | N2 | H2 |
A. ①③ B. ①④ C. ②④ D. ②③
查看答案和解析>>
科目:高中化学 来源:2017届四川外语学院重庆第二外国语学校高三下学期第二次检测理科综合化学试卷(解析版) 题型:选择题
常温下,向10mL0.1mol·L-1的HR溶液中逐滴滴入0.1mol·L-1的NH3·H2O溶液,所得溶液pH及导电性变化如图。下列分析正确的是( )
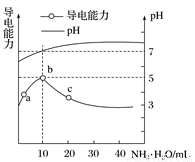
A. HR为强酸 B. a、b两点所示溶液中水的电离程度相同
C. b点溶液中c(NH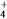 )>c(R-)、c(OH-)>c(H+) D. a~c任意点溶液均有c(H+)·c(OH-)=Kw=1.0×10-14
)>c(R-)、c(OH-)>c(H+) D. a~c任意点溶液均有c(H+)·c(OH-)=Kw=1.0×10-14
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省无锡市高二学业水平模拟(十四)化学试卷(解析版) 题型:推断题
有关物质的转化关系如下图所示(部分物质和条件已略去)。A、C是常见的金属单质,B是黑色有磁性的氧化物,X是黄绿色气体,Y是常见的酸,Z是常见的碱,其焰色反应显黄色。反应①需在高温下进行。

请回答下列问题:
(1) Z的电子式为________。
(2) G的化学式为________。
(3) 写出①的化学方程式:________。
(4) 写出I转化为J的离子方程式:________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省无锡市高二学业水平模拟(十四)化学试卷(解析版) 题型:选择题
下列过程吸收热量的是( )
A. 液氨汽化 B. 镁条燃烧
C. 氢氧化钠溶于水 D. 氧化钙与水反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省枣阳市高一下学期第一次质量检测化学试卷(解析版) 题型:选择题
13C-NMR (核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构KurtWuthrich 等人为此获得2002年诺贝尔化学奖,下面叙述正确的是( )
A. 13C与15N有相同的中子数 B. 13C与C60互为同位素
C. 15N与14N是N元素的两种同位素 D. 15N的核外电子数与中子数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com