
【题目】利用分类和氧化还原反应的知识能实现物质的转化。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:浓硫酸、I2、NaOH、NaCl、HCl
①HBr→Br2的化学方程式:___;
②V2O5(酸性氧化物)→VO![]() 的离子方程式:___。
的离子方程式:___。
(2)利用含碘酸性废水(其中碘主要以IO![]() 形式存在)为原料生产CuI,其流程如图:
形式存在)为原料生产CuI,其流程如图:

①写出“反应Ⅰ”的离子方程式为___;
②写出“反应Ⅱ”的离子方程式:___。
【答案】2HBr+H2SO4(浓)=SO2↑+Br2+2H2O V2O5+6OH-=2VO![]() +3H2O IO
+3H2O IO![]() +3SO2+3H2O=3SO
+3SO2+3H2O=3SO![]() +I-+6H+ 4I-+2Cu2+=2CuI↓+I2
+I-+6H+ 4I-+2Cu2+=2CuI↓+I2
【解析】
(1)①HBr→Br2过程中需要加入氧化剂反应把HBr氧化为Br2,据此分析;
②V2O5为酸性氧化物,在碱性溶液中反应生成相应的可溶性盐而电离出VO![]() ,据此分析;(2)含碘酸性废水中碘主要以IO
,据此分析;(2)含碘酸性废水中碘主要以IO![]() ,加入过量的SO2,会发生离子反应IO
,加入过量的SO2,会发生离子反应IO![]() +3SO2+3H2O=3SO
+3SO2+3H2O=3SO![]() +I-+6H+;反应后的含I-溶液中加入CuSO4溶液,I-和Cu2+发生离子反应4I-+2Cu2+=2CuI↓+I2,过滤即可得到CuI 和含I2的滤液,据此分析。
+I-+6H+;反应后的含I-溶液中加入CuSO4溶液,I-和Cu2+发生离子反应4I-+2Cu2+=2CuI↓+I2,过滤即可得到CuI 和含I2的滤液,据此分析。
(1)①HBr→Br2过程中需要加入氧化剂浓硫酸反应把HBr氧化为Br2,其化学方程式为2HBr+H2SO4(浓)=SO2↑+Br2+2H2O,故答案为:2HBr+H2SO4(浓)=SO2↑+Br2+2H2O;
②V2O5为酸性氧化物,在碱性溶液中反应生成VO![]() ,其离子方程式为V2O5+6OH-=2VO
,其离子方程式为V2O5+6OH-=2VO![]() +3H2O,故答案为:V2O5+6OH-=2VO
+3H2O,故答案为:V2O5+6OH-=2VO![]() +3H2O;
+3H2O;
(2)含碘酸性废水中碘主要以IO![]() ,加入过量的SO2,会发生离子反应IO
,加入过量的SO2,会发生离子反应IO![]() +3SO2+3H2O=3SO
+3SO2+3H2O=3SO![]() +I-+6H+,反应后的含I-溶液中加入CuSO4溶液,I-和Cu2+发生离子反应4I-+2Cu2+=2CuI↓+I2,故答案为:IO
+I-+6H+,反应后的含I-溶液中加入CuSO4溶液,I-和Cu2+发生离子反应4I-+2Cu2+=2CuI↓+I2,故答案为:IO![]() +3SO2+3H2O=3SO
+3SO2+3H2O=3SO![]() +I-+6H+;4I-+2Cu2+=2CuI↓+I2。
+I-+6H+;4I-+2Cu2+=2CuI↓+I2。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为 ( )

A.1:3B.2:3
C.6:1D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中化合物B既能使溴水褪色,又能溶解碳酸钙,D、E均为高分子化合物。根据下图填空:

(1)写出葡萄糖与新制氢氧化铜浊液反应的化学方程式:_____。
(2)A中的官能团有_____(写结构简式)。
(3)E在自然界中可降解,对环境无害,下列说法正确的是___。
A.由A生成E的反应属于加聚反应
B.E的相对分子质量为72
C.E用作一次性快餐盒有助于减少白色污染
(4)在反应①-⑤中,属于取代反应的是_____。写出D和F的结构简式:D_______,F_______。
(5)A跟氢氧化钙作用可制得一种常用的人体补钙剂,测得这种补钙剂的纯净物中钙元素的质量分数为13.0%,其结晶水的含量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧熔融碳酸盐燃料电池是一种高温电池(600﹣700℃),具有效率高、噪音低、无污染等优点。氢氧熔融碳酸盐燃料电池的工作原理如图所示。下列说法正确的是( )
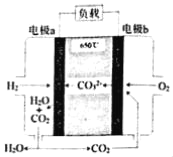
A.电池工作时,熔融碳酸盐只起到导电的作用
B.负极反应式为H2﹣2e﹣+CO32﹣═CO2+H2O
C.电子流向是:电极a﹣负载﹣电极b﹣熔融碳酸盐﹣电极a
D.电池工作时,外电路中流过0.2mol电子,消耗3.2gO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐中常含有少量K+、Ca2+、Mg2+、![]() 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
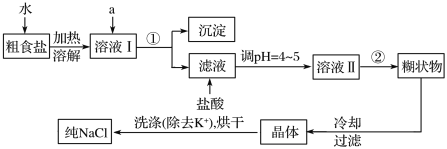
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液
(1)欲依次除去溶液Ⅰ中的Mg2+、![]() 、Ca2+,选出a所代表的试剂,按滴加顺序依次为_______溶液、_________溶液、_________溶液。(填化学式)。
、Ca2+,选出a所代表的试剂,按滴加顺序依次为_______溶液、_________溶液、_________溶液。(填化学式)。
(2)分离操作①中所用到的玻璃仪器除了玻璃棒,烧杯,还需要__________________。
(3)加盐酸的作用__________________
(4)实验室里将粗盐制成精盐的过程中,在溶解的操作中要用到玻璃棒,其作用为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸钠—过氧化氢加合物(xNa2SO4·yH2O2·zH2O)的组成可通过下列实验测定:
①准确称取1.7700g样品,配制成100.00mL溶液A。
②准确量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.5825g。
③准确量取25.00mL溶液A,加适量稀硫酸酸化后,用0.02000mol·L—1KMnO4溶液至终点,消耗KMnO4溶液25.00mL。H2O2与KMnO4反应的离子方程式如下:
2MnO4— + 5H2O2 + 6H+ =2Mn2+ + 8H2O +5O2↑。
通过计算确定样品的组成(写出必要的计算过程)。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 A 与 H2、CO 以物质的量 1∶1∶1 的比例形成 B,B能发生银镜反应,C 分子中只有一种氢,相关物质转化关系如下(含有相同官能团的有机物通常具有相似的化学性质):
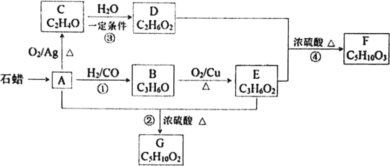
请回答:
(1)有机物 C 的结构简式是________,反应②的反应类型是________。
(2)写出一定条件下发生反应①的化学方程式___________。
(3)下列说法不正确的是________(填字母)。
A.化合物 A 属于烃
B.化合物 D 含有两种官能团
C.用金属钠无法鉴别化合物 F、G
D.A 与 D 一定条件下可以生成 CH3CH2OCH2CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用氯氧化法处理含氰(CN-)废水,一定条件下,氯气和CN-反应生成无毒气体N2和CO2。下列说法不正确的是( )
A.CN-中碳元素的化合价为+2B.该反应的氧化产物是N2
C.反应中氧化剂和还原剂的系数比为5:2D.该反应的还原产物为Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com