

| A. | 锌片逐渐溶解 | B. | 烧杯中溶液逐渐呈蓝色 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 电解质溶液的pH保持不变 |
分析 由图中的铜锌原电池可知,Zn活泼,则Zn作负极,Cu作正极,发生电池反应为Zn+H2SO4═ZnSO4+H2↑,电子由负极流向正极,该装置将化学能转变为电能,以此来解答.
解答 解:A、因Zn作负极,则Zn失去电子而逐渐溶解,故A正确;
B、由发生电池反应为Zn+H2SO4═ZnSO4+H2↑,Cu不反应,则烧杯中溶液为无色,故B错误;
C、Zn作负极,Cu作正极,则电子由锌片通过导线流向铜片,故C错误;
D、由发生电池反应为Zn+H2SO4═ZnSO4+H2↑,电解质溶液的pH减小,故D错误;
故选:A.
点评 本题考查原电池的工作原理,明确电极的判断、电极反应、电池反应、能量转化等即可解答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 在Na2FeO4中Fe显+8价,具有强氧化性,所以能杀菌消毒 | |
| B. | 因为Na2FeO4溶液显碱性,所以能杀菌消毒 | |
| C. | Na2FeO4的还原产物为Fe3+,其易水解产生Fe(OH)3胶体,使水中悬浮物聚沉 | |
| D. | Na2FeO4的还原产物Fe2+ 水解,生成的胶体使水中悬浮物沉降,从而达到消毒目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数(25℃) | Ka=1.75×10-5 | Ka=2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
| A. | 少量CO2通入NaClO溶液中:CO2+H2O+2ClO-═CO32-+2HClO | |
| B. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| C. | 少量SO2通入Na2CO3溶液中:SO2+H2O+2CO32-═SO32-+2HCO3- | |
| D. | 相同浓度NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白磷在冷水中,通入空气也能燃烧 | |
| B. | 酒精灯里的酒精不慎溢出着火,迅速用湿抹布盖灭 | |
| C. | 不能用燃着的木条鉴别氧气、空气和二氧化碳 | |
| D. | 用金刚石去冰箱里的异味 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
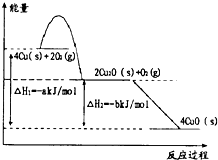 铜及其化合物在工业、农业、科技和日常生活中有广泛应用.
铜及其化合物在工业、农业、科技和日常生活中有广泛应用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 mol | B. | 9 mol | C. | 8 mol | D. | 7 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  向pH=13的NaOH溶液中不断加水稀释 | |
| B. |  向碳酸氢钠溶液中逐滴加入稀盐酸至过量 | |
| C. |  将60℃接近饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出 | |
| D. |  将足量的金属镁片和锌片分别和等质量、相同质量分数的稀硫酸混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 63.00 | B. | 63.60 | C. | 64.00 | D. | 65.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加热或光照时,浓HNO3更易发生分解 | |
| B. | 加催化剂,使氮气和氢气在一定条件下转化为氨气 | |
| C. | 可用浓氨水和氢氧化钠固体快速制取氨气 | |
| D. | H2、I2、HI平衡混和气加压后颜色变深 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com