
| A、(1,3) | ||||
B、(
| ||||
| C、(3,4) | ||||
D、(
|
| x+y |
| 5 |
|
|
| x |
| y |
| 1 |
| 4 |
| x |
| y |
| 3 |
| 2 |
| 1 |
| 4 |
| y |
| x |
| 3 |
| 2 |


科目:高中化学 来源: 题型:
| ||
| pH试纸 |
| ②加入足量氯水 |
| 同时加入氯化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据实验④可推出溶液中不存在NO2-与SO32- |
| B、该溶液中一定含有NO3-、SO42-、NH4+ |
| C、往一定量该溶液中加入足量Ba(NO3)2溶液,静置后往上层清液中滴加硝酸酸化的AgNO3溶液,若有白色沉淀生成,说明溶液中含有Cl- |
| D、根据实验①可推出溶液中含有NO3-或NO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(C)=v(D)=0.2 mol?L-1?s-1 |
| B、x=2 |
| C、B的转化率为75% |
| D、反应前与2 s后容器的压强比为4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
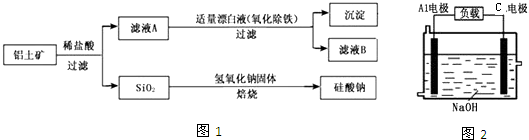

查看答案和解析>>
科目:高中化学 来源: 题型:
| 氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 4.2 |
| 沉淀完全的pH | 3.7 | 9.7 | 6.7 |
| 1 |
| 2 |
| 3 |
| 2 |
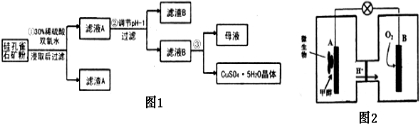
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com