
【题目】关于可逆反应:aA(g)+bB(g)![]() cC(g)+dD(g) ΔH的有关图像如下:
cC(g)+dD(g) ΔH的有关图像如下:
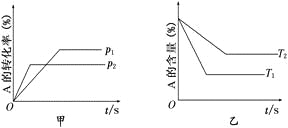
则下列不正确的是
A.p1<p2T1>T2
B.减小压强,正逆反应速率都减小,平衡右移
C.ΔH>0 ΔS>0
D.升高温度,混合气体的平均摩尔质量增大
【答案】D
【解析】
A.根据图甲可知在压强为P2时首先达到平衡,则P2>P2,根据图2可知在温度为T1时显达到平衡,所以T1>T2,因此选项A正确;
B. 减小压强,正逆反应速率都减小,根据图1可知增大压强,A的转化率降低,则平衡向平衡左移,减小压强,平衡向右移动,正确;
C.由于升高温度,A的含量降低,则该反应的正反应是吸热反应,,则ΔH>0 ,减小压强,A的转化率增大,则该反应的正反应是气体体积增大的反应,所以ΔS>0,正确;
D.升高温度,平衡向正反应方向移动,而正反应方向是气体体积增大的反应,所以升高温度,混合气体的物质的量增大,而质量不变,因此混合气体的平均摩尔质量减小,错误。
故选D。


科目:高中化学 来源: 题型:
【题目】微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如下图所示,下列说法不正确的是

A. 该电池在高温下工作的速度更快
B. HS-在硫氧化菌作用下转化为SO42-的反应是:HS-+4H2O-8e-= SO42-+9H+
C. b是电池的负极
D. 若该电池有0.45 mol 电子转移,则有0.45 mol H+向左通过质子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究大气中含硫化合物(主要是H2S和SO2)的转化具有重要意义。
(1)H2S资源化利用途径之一是回收能量并得到单质硫,如图为质子膜H2S燃料电池的示意图。
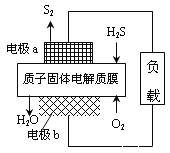
①电极a为电池的_______极,电极b上发生的电极反应为:______________________。
②每17gH2S参与反应,有_____molH+经质子膜进入_____极区。
(2)低浓度SO2废气的处理是工业难题,目前常用的方法如下:
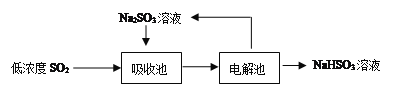
①Na2SO3溶液吸收SO2的化学方程式是____________________________________。
②如果用含等物质的量溶质的下列各溶液分别吸收SO2,则理论吸收量最多的是(____)
A.Na2SO3B.Na2S C.Ba(NO3)2 D.酸性KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了清理路面积雪,人们常使用一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54mol电子。
(1)该融雪剂的化学式是____,该物质中化学键类型是______,电子式是______。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是__________;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8e-稳定结构,该分子的结构式为_________,电子式为_______,化学键类型为_________(填“离子键”“非极性共价键”或“极性共价键”)。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:不加热时生成____,其化学键类型为___;加热时生成_____,其化学键类型为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是由常见元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(部分物质已经略去)。其中A、B、D在常温下均为无色无味的气体,C是能使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)写出C→E的化学方程式: 。
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为: ,干燥C常用 (填写试剂名称)。
(3)E物质遇到D物质时,会观察到 现象,若用排水法收集F,则最终集气瓶中收集到的气体为 (填写物质的化学式)。
(4)写出A→D的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)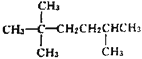 ,请用系统命名法对该物质进行命名:___。若该烃为一单烯烃的加成产物,则单烯烃可能有___种结构。
,请用系统命名法对该物质进行命名:___。若该烃为一单烯烃的加成产物,则单烯烃可能有___种结构。
(2)某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%,A的分子式为___。
(3)若25℃时CH3COOH的电离平衡常数Ka=1.8×10-5mol·L-1,向aLCH3COOH溶液中加入bmol CH3COONa,混合液恢复至25℃时呈中性,则原 CH3COOH溶液的物质的量浓度为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料,某探究小组利用下列反应和装置制备一硝基甲苯。
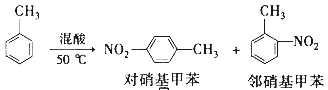
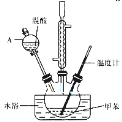
实验中可能用到的数据:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:①按体积比1∶3配制浓硫酸与浓硝酸混合物40mL;
②在三颈瓶中加入15mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60g。
请回答下列问题:
(1)仪器A的名称是___,使用该仪器前必须进行的操作是___。
(2)若实验后在三颈瓶中收集到的产物较少,可能的原因是___。
(3)分离反应后产物的方案如下:

其中,操作1的名称为____,操作2中需要使用下列仪器中的____(填字母)。
a.冷凝管 b.酒精灯 c.温度计 d.分液漏斗 e.蒸发皿
(4)该实验中一硝基甲苯的产率为___(保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知煤转化成水煤气及其燃烧过程的能量变化如下图,则下列说法正确的是
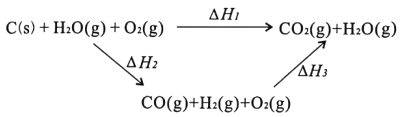
A.△H1-△H2+△H3=0
B.△H1<△H2
C.由△H3可知,该步反应的反应物键能总和大于生成物的键能总和
D.若用C(s)和H2O(l)转化为H2(g)和CO(g),则△H2变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图(铁架台、铁夹、酒精灯等未画出):
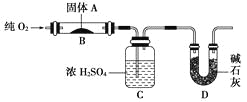
取17.1 g A放入装置中,通入过量O2燃烧,生成CO2和H2O,请回答下列有关问题:
(1)通入过量O2的目的是______________________________________________。
(2)C装置的作用是__________________________________________;
D装置的作用是_____________________________________________。
(3)通过该实验,能否确定A中是否含有氧原子?________。
(4)若A的摩尔质量为342 g/mol,C装置增重9.99 g,D装置增重26.4 g,则A分子式为____________。
(5)写出A燃烧的化学方程式_____________________________________。
(6)A可发生水解反应,1 mol A可水解生成2 mol同分异构体,则A在催化剂作用下水解的化学方程式为_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com