
【题目】氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:

依据上图,完成下列填空:
(1)在电解过程中,所发生的反应方程式为______________________________________。与电源_______极相连的电极附近溶液滴入酚酞显红色。阳极产物是______________,实验室用__________________________检验该物质。
(2)如果粗盐中SO42含量较高,必须添加钡试剂除去SO42,该试剂可以是_____________________。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2 d.BaCO3
(3)为有效除去Ca2+、Mg2+、SO42,加入试剂的合理顺序为__________________。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
【答案】2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑ 负 氯气 湿润的淀粉碘化钾试纸 c bc
2NaOH+Cl2↑+H2↑ 负 氯气 湿润的淀粉碘化钾试纸 c bc
【解析】
(1)电解饱和食盐水的原理方程式为:2NaCl+2H2O==2NaOH+H2↑+Cl2↑,电解食盐水,与正极相连为阳极,生成氯气,与电源负极相连为阴极,生成氢气和NaOH;
(2)添加钡试剂除去SO42-,注意不能引入新的杂质;
(3)用可溶性的碳酸钠除去钙离子,用NaOH除去镁离子。
(1)电解氯化钠溶液时,阳极是氯离子失电子生成氯气的过程,电极反应式为2Cl--2e-=Cl2↑,阴极是氢离子得电子生成氢气的过程,发生电极反应:2H++2e-=H2↑,该极消耗氢离子,电极附近溶液pH升高,生成氢氧化钠,总反应为![]() 2NaCl+2H2O==2NaOH+H2↑+Cl2↑,实验室用湿润的淀粉碘化钾试纸检验该物质.
2NaCl+2H2O==2NaOH+H2↑+Cl2↑,实验室用湿润的淀粉碘化钾试纸检验该物质.
故答案为: 2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑; 负 ;氯气 ;湿润的淀粉碘化钾试纸
2NaOH+Cl2↑+H2↑; 负 ;氯气 ;湿润的淀粉碘化钾试纸
(2)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂选择的原则是不引入难以除去的杂质离子,故答案为C
(3)Ca2+、Mg2+等杂质与碳酸钠、NaOH反应转化为沉淀,除去SO42-必须用钡试剂,由于钡试剂本身就含有杂质,因此钡试剂不能放在最后一步;
故答案为:bc.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理(平衡移动原理)解释的是
①铁在潮湿的空气中容易生锈
②二氧化氮与四氧化氮的平衡体系,加压缩小体积后颜色加深
③实验室可用排饱和食盐水的方法收集氯气
④钠与氯化钾共融制备钾 Na(l)+KCl(l)![]() K(g)+NaCl(l)
K(g)+NaCl(l)
⑤开启啤酒瓶后,瓶中马上泛起大量泡沫
A. ③④ B. ①② C. ①⑤ D. ①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下列两种方法制取氯气:①用含HCl 146g的浓盐酸与足量的MnO2反应;②用87g MnO2与足量的浓盐酸反应,则所得Cl2质量
A. ①比②多B. ②比①多C. 一样多D. 无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工厂生产的氯气和氢气可以进一步用于生产盐酸,主要过程如下:

(1)其中关键的一步为氯气和氢气在燃烧管口燃烧生成HCl,氯气有毒,应采取的措施是____。合成盐酸厂要求合成气中的HCl的含量要大于97%,试用最简便的方法进行分析是否含量大于97%____。
(2)氯碱工厂生产的氯气和氢氧化钠溶液可以用于制取“84消毒液”,反应的化学方程式为__。
(3)某同学欲证明盐酸与氯化氢气体性质不同,他分别向A、B、C三支洁净试管中各放入一片干燥的蓝色石蕊试纸,然后往A试管内加入盐酸,试纸显___色,往B试管中通入干燥的氯化氢气体,试纸显___色.最后向C试管中加入物质___(填化学式),他之所以加入这种物质的理由是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀废液中Cr2O7可通过下列反应转化成铬黄(PbCrO4):
Cr2O![]() (aq)+2Pb2+(aq)+H2O(l)
(aq)+2Pb2+(aq)+H2O(l) ![]() 2PbCrO4(s)+2H+(aq) ΔH<0
2PbCrO4(s)+2H+(aq) ΔH<0
该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是 ( )。
A. 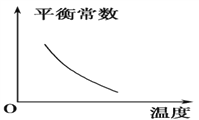 B.
B. 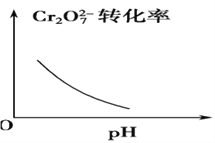
C.  D.
D. 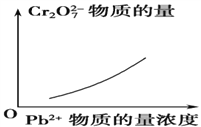
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:X(g)+2Y(g)![]() 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是
A. 容器内压强不随时间变化
B. 容器内气体密度不随时间变化
C. 容器内X、Y、Z的浓度之比为1:2:2
D. 单位时间消耗0.1molX同时生成0.2molZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种化合物,它们之间的反应关系如下所示:
①A+B→C+E ②C+NaOH→蓝色沉淀D+F ③D![]() A+E ④F+Ba(NO3)2→白色沉淀+NaNO3
A+E ④F+Ba(NO3)2→白色沉淀+NaNO3
回答下列问题:
(1)写出它们的化学式:
A.____________B. ____________C. ____________D. ____________E. ____________F. ____________。
(2)写出①、②、③、④反应的化学方程式,属于离子反应的只写离子方程式:
①____________________________________;
②____________________________________;
③____________________________________;
④____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E 都是前20号元素中的常见元素,且核电荷数递增。A原子没有中子;B原子次外层电子数与最外层电子数之差等于电子层数;C元素是地壳中含量最高的元素;4.6gD单质与足量盐酸作用可产生2.24LH2(标准状态下);E的一价阴离子的核外电子排布与Ar的核外电子排布相同。请回答下列问题:
(1)写出A、B、D的元素符号:A______;B_____;D______。
(2)C离子的电子式_______;E的离子结构示意图_______。
(3)写出电解D、E形成化合物的水溶液的化学反应方程式______。
(4)工业上将E的单质通入石灰乳[Ca(OH)2]制取漂粉精,化学反应方程式为______。漂粉精溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的某种物质,该化学反应方程式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com