
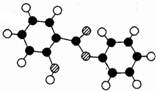
 萨罗是一种消毒剂,它的分子式为C13H10O3,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等):
萨罗是一种消毒剂,它的分子式为C13H10O3,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等): .
.
 或
或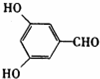 (任写一种).
(任写一种). 分析 (1)萨罗的分子式为C13H10O3,由分子式可知,模型中黑色球代表碳元素,白色球代表氢原子,斜线白色球为氧原子.根据碳的四价结构,可知结构中环为苯环,根据氧原子的二价结构可知,连接两个苯环的基团为酯基,有1个-OH连接苯环;
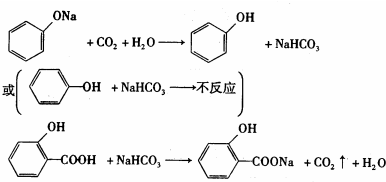
(2)根据强酸制弱酸设计,羧酸酸性比碳酸强,碳酸酸性比苯酚强;
(3)水杨酸为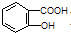 .根据题意知,该有机物中含有-CHO,不含酯的结构,含有两个与苯环相连的羟基.
.根据题意知,该有机物中含有-CHO,不含酯的结构,含有两个与苯环相连的羟基.
解答 解:(1)萨罗的分子式为C13H10O3,由分子式可知,模型中黑色球代表碳元素,白色球代表氢原子,斜线白色球为氧原子.根据碳的四价结构,可知结构中环为苯环,根据氧原子的二价结构可知,连接两个苯环的基团为酯基,有1个-OH连接苯环.所以萨罗的结构简式 ,
,
故答案为: ;
;
(2))要证明酸的相对强弱,一般利用强酸与弱酸的盐反应,故可利用下列反应来证明三者的相对强弱: ,
,
故答案为: ;
;
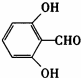
(3)能发生银镜反应证明有醛基,不能发生水解反应说明无酯基,1 mol该同分异构体能与2 mol NaOH发生反应则说明有两个酚羟基,只能生成两种一氯代产物说明具有较好的对称性,符合条件的同分异构体有如下两种: 和
和 ,
,
故答案为:2; 或
或 .
.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生综合运用化学知识的能力的考查,注意根据有机物球棍模型判断有机物结构简式为解答该题的关键,并把握有机物官能团的性质,题目难度不大.


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子组成相差一个或几个“-CH2-”原子团的物质互为同系物,它们有相似的化学性质和不同的物理性质 | |
| B. | 甲烷是烷烃中碳的含量最低的,也是最简单的烃 | |
| C. | 不带支链的烃,其分子都是直线型的 | |
| D. | 常温时烷烃的同系物,只有四种呈气态 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
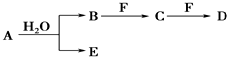
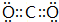 ;D中所含化学键的类型为离子键、共价键.
;D中所含化学键的类型为离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3s1和3s23p4 | B. | 3s23p4 和2s22p4 | ||
| C. | 3s2和2s22p5 | D. | 2s22p2 和2s22p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
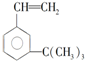 有如下性质:
有如下性质: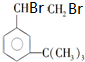 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2与H2O反应产生O2:2Na2O2+2H2O═4Na++4OH-+O2↑ | |
| B. | 用氢氧化钠溶液去除铝条表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| C. | 向铜片中滴加浓硫酸并加热,有刺激性气味气体产生:Cu+4H++SO42- $\frac{\underline{\;\;△\;\;}}{\;}$Cu2++SO2↑+2H2O | |
| D. | 向明矾溶液中滴入少量氢氧化钡溶液:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
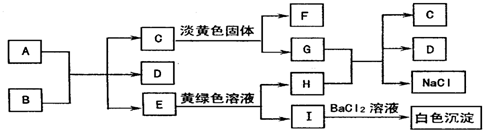
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com