
| A. | 滴加KI-淀粉溶液变为蓝色 | |
| B. | 该溶液中Cu2+、NH4+、SO4-、Cl- 可以大量共存 | |
| C. | 与硝酸酸化的AgNO3溶液反应有沉淀生成并放出气体 | |
| D. | 配制该溶液时,将FeBr2粉末溶解在HBr溶液中,并加入少量铁钉 |
分析 A.KI与FeBr2不反应不能生成碘单质;
B.离子之间不反应,且与FeBr2不反应;
C.亚铁离子与硝酸发生氧化还原反应生成NO,溴离子与银离子反应生成AgBr;
D.FeBr2粉末溶解后溶液中溴化亚铁水解变浑浊,需要加入对应酸抑制水解,亚铁离子被空气中氧气氧化,加入铁粉防止亚铁离子被氧化.
解答 解:A.KI与FeBr2不反应,则滴加KI-淀粉溶液无现象,故A错误;
B.离子之间不反应,且与FeBr2不反应,则离子之间可大量共存,该溶液中Cu2+、NH4+、SO4-、Cl- 可以大量共存,故B正确;
C.亚铁离子与硝酸发生氧化还原反应生成NO,溴离子与银离子反应生成AgBr沉淀,则反应有沉淀生成并放出气体,故C正确;
D.配制该溶液时,将FeBr2粉末溶解在HBr溶液中防止水解,并加入少量铁钉防止亚铁离子被氧化,故D正确;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度中等.


科目:高中化学 来源: 题型:解答题
| 装置 | 现象 | 结论及解释 |
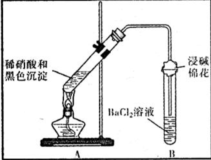 | ①A试管中黑色沉淀逐渐溶解 ②A试管上方出现红棕色气体 ③B试管中出现白色沉淀 | a.现象②说明褐色沉淀具有 还原性性. b.试管B中产生白色沉淀的总反应的离子方程式为 NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
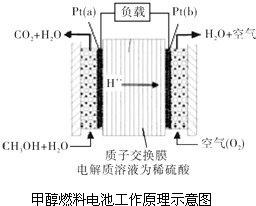 科学家预言,燃料电池将是21世纪获得电能的重要途径.近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过.其工作原理的示意图如图所示:
科学家预言,燃料电池将是21世纪获得电能的重要途径.近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过.其工作原理的示意图如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使它转化为较稳定物质,便于保存和运输 | |
| B. | 增强漂白和消毒作用 | |
| C. | 使转化为较易溶于水的物质 | |
| D. | 增加氯的质量分数,有利于漂白、消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 molN2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)$?_{500℃、30Mpa}^{催化剂}$2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | HCl和NaOH反应的中和热△H=-57.3 kJ•mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ•mol-1 | |
| D. | 碳酸氢钠溶液中加入过量Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
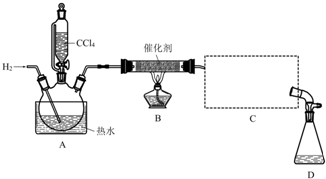
| 物质 | 相对分子质量 | 密度/(g•mL-1) | 沸点/℃ | 水中溶解性 |
| CHCl3 | 119.5 | 1.50 | 61.3 | 难溶 |
| CCl4 | 154 | 1.59 | 76.7 | 难溶 |
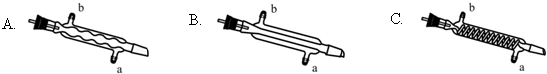
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 邻-二溴苯只有一种 | |
| B. | 苯分子中所有原子在同一平面上 | |
| C. | 二甲苯没有同分异构体 | |
| D. | 苯既能发生加成反应也能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 维生素C不具有还原性 | |
| B. | 上述过程中砷元素发生还原反应 | |
| C. | 上述过程中+5价砷类物质作还原剂 | |
| D. | 1 mol+5价砷完全转化为+3价砷,共失去2 mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com