
ÔÚĘĒÓÐAgNO3ĄĒHBrĄĒNa2CO3ĄĒCaCl2ĄĒNaIÎåÖÖÎÞÉŦČÜŌšĩÄĘÔžÁÆŋÉÏĢŽ·ÖąðĖųÓÐĒŲĄŦĒÝĩÄąāšÅĄĢ―ŦËüÃĮÁ―Á―ŧėšÏĢŽēúÉúĩÄÏÖÏóČįÏÂąíËųÁÐĢš
| ĒŲ | ĒÚ | ĒÛ | ĒÜ | ĒÝ | |
| ĒŲ | ĄŠĄŠ | ĄüÎÞÉŦ | Ąý°ŨÉŦ | Ąý°ŨÉŦ | ÎÞÃũÏÔÏÖÏó |
| ĒÚ | ĄüÎÞÉŦ | ĄŠĄŠ | ÎÞÃũÏÔÏÖÏó | ĄýĩŧÆÉŦ | ÎÞÃũÏÔÏÖÏó |
| ĒÛ | Ąý°ŨÉŦ | ÎÞÃũÏÔÏÖÏó | ĄŠĄŠ | Ąý°ŨÉŦ | ÎÞÃũÏÔÏÖÏó |
| ĒÜ | Ąý°ŨÉŦ | ĄýĩŧÆÉŦ | Ąý°ŨÉŦ | ĄŠĄŠ | ĄýŧÆÉŦ |
| ĒÝ | ÎÞÃũÏÔÏÖÏó | ÎÞÃũÏÔÏÖÏó | ÎÞÃũÏÔÏÖÏó | ĄýŧÆÉŦ | ĄŠĄŠ |
| ―áÂÛ |
 ĩžŅ§ÓëēâĘÔÏĩÁÐīð°ļ
ĩžŅ§ÓëēâĘÔÏĩÁÐīð°ļ зĮ·ē―ĖļĻģåīĖ100·ÖÏĩÁÐīð°ļ
зĮ·ē―ĖļĻģåīĖ100·ÖÏĩÁÐīð°ļ
| Äęžķ | ļßÖÐŋÎģĖ | Äęžķ | ģõÖÐŋÎģĖ |
| ļßŌŧ | ļßŌŧÃâ·ŅŋÎģĖÍÆžöĢĄ | ģõŌŧ | ģõŌŧÃâ·ŅŋÎģĖÍÆžöĢĄ |
| ļßķþ | ļßķþÃâ·ŅŋÎģĖÍÆžöĢĄ | ģõķþ | ģõķþÃâ·ŅŋÎģĖÍÆžöĢĄ |
| ļßČý | ļßČýÃâ·ŅŋÎģĖÍÆžöĢĄ | ģõČý | ģõČýÃâ·ŅŋÎģĖÍÆžöĢĄ |
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš

| ||
| ||
ēéŋīīð°ļšÍ―âÎö>>
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš
| O | - 3 |
| O | 2- 3 |
ēéŋīīð°ļšÍ―âÎö>>
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš
| [CO] | [CO2] |
ēéŋīīð°ļšÍ―âÎö>>
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš2015―ėļĢ―ĻĘĄļĢÖÝĘаËÏØļßķþÉÏŅ§ÆÚÆÚÄĐŋžĘÔŧŊŅ§ĘÔūíĢĻ―âÎö°æĢĐ ĖâÐÍĢšĖîŋÕĖâ
ĢĻ1ĢĐŌŅÖŠĢšC3H8(g)+5O2(g) ===3CO2(g)+4H2O(1) ĄũH=Ģ2220.0kJ/mol
H2O(1) ===H2O(g)ĢŧĄũH=+44.0kJ/mol
ÐīģöąûÍéČžÉÕÉúģÉCO2šÍÆøĖŽËŪĩÄČČŧŊŅ§·―ģĖĘ― ĄĢ
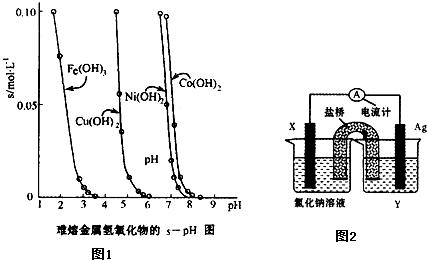
ĢĻ2ĢĐÔÚČįÍžËųĘūĩÄĘĩŅéŨ°ÖÃÖÐĢŽEΊŌŧÕÅÓÃĩí·ÛĩâŧŊžØČÜŌšČóĘŠĩÄÂËÖ―ĢŽCĄĒDΊžÐÔÚÂËÖ―Á―ķËĩÄēŽžÐĢŽXĄĒY·ÖąðΊֹÁũĩįÔīĩÄÁ―žŦĄĢÔÚAĄĒBÖÐģäÂúAgNO3ČÜŌššóĩđÁĒÓÚĘĒÓÐAgNO3ČÜŌšĩÄËŪēÛÖÐĢŽÔŲ·ÖąðēåČëēŽĩįžŦĄĢĮÐķÏĩįÔīŋŠđØS1ĢŽąÕšÏŋŠđØS2ĢŽÍĻÖąÁũĩįŌŧķÎĘąžäšóĢŽBĩįžŦÖĘÁŋÔöÖØĢŽAžŦēúÉúÎÞÉŦÆøĖåĄĢĮëŧØīðÏÂÁÐÎĘĖâĢš
ĒŲ ÐīģöDĩįžŦ·īÓĶĘ―ĢšĄĄĄĄĄĄĄĄĄĄĄĄĄĄ Ģŧ
ĒÚÐīģöËŪēÛÖÐĩį―âAgNO3ČÜŌšŨÜ·īÓĶĩÄĀëŨÓ·―ģĖĘ―Ģš ĢŽŌõžŦÔöÖØ2.16 gĢŽÔōŅôžŦÉÏ·ÅģöĩÄÆøĖåÔÚąęŨžŨīŋöÏÂĩÄĖåŧýĘĮ____ _LĄĢ

ēéŋīīð°ļšÍ―âÎö>>
°ŲķČÖÂÐÅ - Á·Ï°ēáÁÐąí - ĘÔĖâÁÐąí
šþąąĘĄŧĨÁŠÍøÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻÆ―ĖĻ | ÍøÉÏÓКĶÐÅÏĒūŲąĻŨĻĮø | ĩįÐÅÕĐÆūŲąĻŨĻĮø | ÉæĀúĘ·ÐéÎÞÖũŌåÓКĶÐÅÏĒūŲąĻŨĻĮø | ÉæÆóĮÖČĻūŲąĻŨĻĮø
ÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻĩįŧ°Ģš027-86699610 ūŲąĻÓĘÏäĢš58377363@163.com