
| 催化剂 |
| 加热 |
A、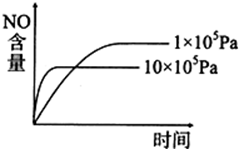 |
B、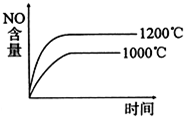 |
| C、NO难溶于水,可以用排水法收集,但不可以用排空气法 |
| D、当生成标准状况下3.36L的氧气时,该反应转移0.6mole |


科目:高中化学 来源: 题型:
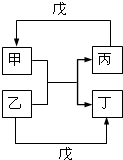 甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( )
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( )| 甲 | 乙 | 戊 | |
| A | FeCl3溶液 | Cu | Cl2 |
| B | Na2SO3 | H2SO4 | NaOH |
| C | Na2O2 | CO2 | Na2O |
| D | SiO2 | Na2CO3 | CO2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
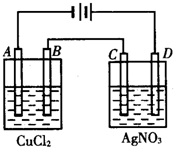 如图为以惰性电极进行电解.完成下列问题
如图为以惰性电极进行电解.完成下列问题查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、绿色变浅 | B、绿色变深 |
| C、变黄 | D、不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度 | B、减低压强 |
| C、使用催化剂 | D、及时分离出氨 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com