
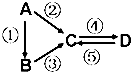
 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
| ||
| △ |
| ||
| △ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、①②⑥⑦ | B、③⑤⑦⑧ |
| C、①③⑦⑧ | D、③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 光 |
| A、蒸馏法 | B、水洗分液法 |
| C、过滤法 | D、有机溶剂萃取法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、20% | B、40% |
| C、60% | D、80% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、回收废旧电池的目的是为了回收废旧电池中的碳棒 |
| B、碘元素是人体必需的微量元素,所以人每天要摄入大量的碘元素 |
| C、“地沟油”虽然对人体有害,但对“地沟油”进行分馏可制得汽油、煤油,达到变废为宝的目的 |
| D、镀锌铁片的镀层受损,还能起到保护铁的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaX NaY NaZ |
| B、NaX NaZ NaY |
| C、NaY NaZ NaX |
| D、NaZ NaY NaX |
查看答案和解析>>
科目:高中化学 来源: 题型:
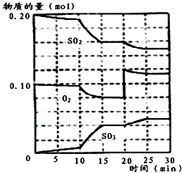 已知一定条件下在1L的密封容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g),△H<0,反应过程中SO2、O2、SO3物质的量变化如图,请根据图示回答下列问题:
已知一定条件下在1L的密封容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g),△H<0,反应过程中SO2、O2、SO3物质的量变化如图,请根据图示回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com