
下列说法正确的是
A.原子最外层电子数为2的元素一定处于周期表ⅡA族
B.主族元素X、Y能形成XY2型化合物,则X与Y 的原子序数之差可能为2或5
C.氯化氢的沸点比氟化氢的沸点高
D.同主族元素形成的氧化物的晶体类型均相同
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:2016届江苏省扬州市高三上学期期中检测化学试卷(解析版) 题型:选择题
下列设计的实验方案能达到实验目的的是
A.制备干燥的NH3:加热浓氨水,将生成的气体通过盛有浓硫酸的洗气瓶
B.提纯含有少量HCl的CO2:将混合气体依次通过盛有饱和碳酸钠溶液、浓硫酸的洗气瓶
C.检验食盐中是否含有碘酸钾:取少量的食盐溶液,加稀硫酸酸化,再滴入淀粉溶液,观察实验现象
D.探究温度对化学平衡移动的影响:将盛有NO2和N2O4混合气体的烧瓶,先后置于冷水和热水中,观察烧瓶中气体颜色的变化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北成安一中、永年二中高一上期中联考化学试卷(解析版) 题型:实验题
某同学购买了一瓶××牌“84消毒液”,查阅相关资料和消毒液包装说明得到如下信息:“84消毒液”:含25%NaClO 1 000 mL、密度1.19 g·cm-3。
请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为 mol·L-1(保留两位有效数字)。
(2)某实验需用480 mL含25%NaClO的消毒液。该同学参阅该“84消毒液”的配方,欲用NaClO固体配制该消毒液。
①下列说法正确的是 。

A.如上图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制
C.利用久置的NaClO来配制可能导致结果偏低
D.需要称量的NaClO固体质量为143 g
②在配制过程中,下列操作可能使配制的溶液的浓度偏大的是 。
A.烧杯中溶液转移到容量瓶中时,未洗涤烧杯
B.定容时,俯视刻度线
C.定容时,仰视刻度线
D.移液时,有少量液体溅出
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(文)化学试卷(解析版) 题型:填空题
有四种常见药物 ①阿司匹林 ②青霉素 ③胃舒平 ④麻黄碱。请回答:
(1)某同学胃酸过多,应选用的药物是________(填序号),抗酸药是治疗胃酸过多的一类药品,请写出一种抗酸药(有效成分是碳酸钙)中和胃酸过多的化学反应方程式:_____________。
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是_________(填序号)。
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是_________(填序号)。
(4)滥用药物会导致不良后果,如过量服用_________(填序号)会出现水杨酸中毒,应立即停药,并静脉注射NaHCO3 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省东阳市高三上学期12月月考化学试卷(解析版) 题型:推断题
Ⅰ.A、B、C、D是四种短周期元素,它们的原子序数依次增大。其中A、D元素同主族,B、C元素同周期;由A、B、C、D中的两种元素可形成原子个数比为1:1的多种化合物,甲、乙、丙、丁为其中的四种,它们的元素组成如下表所示:

常温下,甲物质为气体,密度略小于空气;乙物质为液体;丙物质和丁物质为固体且都为离子化合物。请填写下列空白:
(1)丙物质的电子式为 ,丁物质中阴离子与阳离子的个数之比为 ,写出丁与水反应的离子方程式 。
(2)若标准状况下5.6L甲物质完全燃烧放出的热量为QKJ,试写出表示甲物质燃烧热的热化学方程式 。
(3)B、C两种元素按原子个数比为1:2可形成化合物戊,A、C、D三种元素按原子个数比为1:1:1可形成化合物己,则己与戊按物质的量之比为3:2完全反应后的溶液中各离子浓度的大小关系为 。
Ⅱ.下图是无机物A~N在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。N中只含有两种元素,N可作为工业生产C的原料。

请填写下列空白:
(1)单质G: 。
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是 (填写序号)。
(3)反应⑩的离子方程式是 。
(4)反应④的离子方程式是 。
(5)将化合物D 与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾)。同时还生成KNO2和H2O。该反应的化学方程式是: 。
(6)现有1molN参加反应,假设各步反应均完全,生成C的质量为490g,生成G的质量为224g,则反应①的化学方程式为
查看答案和解析>>
科目:高中化学 来源:2016届四川省资阳市高三上学期第一次诊断性测试理综化学试卷(解析版) 题型:填空题
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会对环境造成严重影响。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为______________。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
①取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如右图所示,则上述CO2转化为甲醇的反应热△H3___________0(填“>”、“<”或“=”),该反应的平衡常数表达式为_____________。

②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如右图所示。

试回答:0~10 min内,氢气的平均反应速率为______________mol/(L·min)。第10 min后,若向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时CH3OH(g)的体积分数___________(填“变大”、“减少”或“不变”)。
(3)脱硫。
①有学者想利用如右图所示装置用原电池原理将SO2转化为重要的化工原料,A、B是惰性电极。
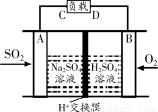
则电子流出的电极为_____________(用A或B表示),A极的电极反应式为_____________。
②某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物,可作为化肥。硫酸铵和硝酸铵的水溶液pH<7,其原因用离子方程式表示为__________;常温下,向一定物质的量浓度的硝酸铵溶液中滴加适量的氨水溶液,使溶液中的NO3-和NH4+的物质的量浓度相等,则溶液的pH 7(填写“>”“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期期中测试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.1 mol N2的质量为28g/mol
B.3.01×1023个SO2分子的质量为32g
C.Cl2的摩尔质量为71g
D.标准状况下1 mol任何物质体积均为22.4L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市四校高二上学期期中联考化学试卷(解析版) 题型:选择题
下列生产、生活等实际应用,不能用勒夏特列原理解释的是
A.合成氨工业通常采用20 MPa~50 MPa压强,以提高原料的利用率
B.合成氨工业中采用500℃反应温度,有利于氨的合成
C.合成三氧化硫过程中使用过量的氧气,以提高二氧化硫的转化率
D.阴暗处密封有利于氯水的储存
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期期中测试化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列判断错误的是
A.NA个H+的质量为1 g
B.2 L 0.5 mol/L Na2SO4溶液中含NA个Na+
C.32 g O2中含有2NA个氧原子
D.标准状况下,1 mol H2O中含有NA个分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com