
分析 苯、1-己烯都不溶于水,1-己烯可与溴水反应,乙醇、甲醛溶液和苯酚溶液可用溴水鉴别,以此解答该题.
解答 解:(1)可加入溴水,苯分层,色层在上层,乙醇无现象,1-己烯可使溴水褪色,溶液分层,甲醛可使溴水褪色,溶液不分层,苯酚与溴水发生取代反应生成白色沉淀,
答:加入溴水鉴别;
(2)能与溴水发生反应的为1-己烯、甲醛溶液和苯酚溶液,涉及反应的方程式为,CH2=CH(CH2)3CH3+Br2→CH2BrCHBrCH2CH2CH2CH3、HCHO+H2O+Br2→HCOOH+2HBr、 ,
,
答:有关反应的化学方程式为CH2=CH(CH2)3CH3+Br2→CH2BrCHBrCH2CH2CH2CH3、HCHO+H2O+Br2→HCOOH+2HBr、 .
.
点评 本题考查有机物的鉴别,为高频考点,侧重于学生的分析、实验能力的考查,注意把握有机物的官能团的性质,把握性质的异同,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A>B>C>D | |
| B. | 离子半径:D(n+1)->Cn->B(n+1)+>An+ | |
| C. | 原子序数:b>a>c>d | |
| D. | 金属性:B>A,气态氢化物稳定性:D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2、NH3、HCl | B. | O2、NO、NO2 | C. | O2、H2、N2 | D. | CO2、H2、SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
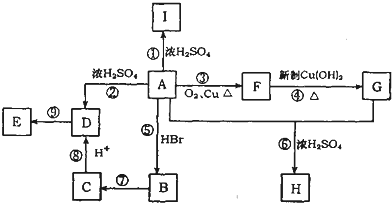
 .
. ;写出反应⑦的化学方程式:
;写出反应⑦的化学方程式: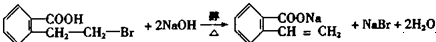 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
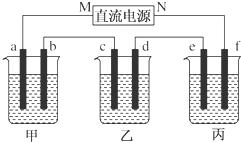
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com