
【题目】关于0.1mol/LH2SO4溶液的叙述错误的是
A.1L该溶液中含有H2SO4的质量为9.8g
B.0.5L该溶液中氢离子的物质的量浓度为0.2mol·L-1
C.从1L该溶液中取出100mL,则取出溶液中H2SO4的物质的量浓度为0.01mol/L
D.取该溶液10mL,加水稀释至100mL后H2SO4的物质的量浓度为0.01mol/L
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】查表得知HI的稳定性远不如HF,在HI的合成过程中存在下列平衡:
①H2(g)+I2(g)![]() 2HI(g) △H=-14.9kJ/mol
2HI(g) △H=-14.9kJ/mol
②H2(g)+I2(s)![]() 2HI(g) △H=+26.48kJ/mol
2HI(g) △H=+26.48kJ/mol
向2L的密闭容器中,加入1 mol H2(g)和2 molI2(g)发生反应①,达到平衡后,测得放热5.96kJ,将容器压缩体积至1L,当各气体组分浓度不再改变时,测反应放出的热量,就可以计算出平衡体系中I2(g)的体积分数。很据反应①②还可以得出I2(g)![]() I2(s) △H=-41.38kJ/mol。上面描述中,没有涉及到哪位化学家提出的理论( )
I2(s) △H=-41.38kJ/mol。上面描述中,没有涉及到哪位化学家提出的理论( )




A.阿伏加德罗 B.门捷列夫 C.盖斯 D.勒夏特列
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B混合于2L的密闭容器中发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),经5min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1 mol/(L·min)。
xC(g)+2D(g),经5min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1 mol/(L·min)。
求:(1)此时A的浓度及反应开始前容器中A、B的物质的量;
(2)B的平均反应速率;
(3)x的值。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质之间通过一步就能实现如图所示转化的是( )
物质编号 | 物质转化关系 | a | b | c | d |
① |
| Na2O | Na2O2 | Na | NaOH |
② | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
③ | FeCl2 | FeCl3 | Fe | CuCl2 | |
④ | NO | NO2 | N2 | HNO3 |
A.①③ B.①② C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴单质具有广泛的工业价值,查阅资料知:Br2的沸点为59℃,微溶于水,有毒性。某化学小组模拟工业流程从浓缩的海水中提取液溴,主要实验装置(夹持装置略去)及操作步骤如下:

A B C
①连接A与B,关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③进行步骤②的同时,向B中通入足量SO2;
④关闭b,打开a,再通过A向B中缓慢通入足量Cl2;
⑤将B中所得液体进行蒸馏,收集液溴。
请回答:
(1)判断步骤①中反应已经结束的最简单方法为 。
(2)步骤②中鼓入热空气的作用为 ;
步骤③B中发生的主要反应的离子方程式为 。
(3)综合分析步骤①、②、③和④,这四步操作的最终目的为 。
(4)此实验中尾气可用 (填选项字母)吸收处理。
a.水 b.浓硫酸 c.NaOH溶液 d.饱和NaCl溶液
(5)步骤⑤中,蒸馏用到的玻璃仪器除酒精灯、温度计、尾接管、锥形瓶外,还有________和 ;要达到提纯溴的目的,操作中应控制的关键条件为 。
(6)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸,再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C中反应生成了NaBr、NaBrO3等,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中,一定条件下进行如下反应:NO(g)+CO(g)![]() 1/2N2(g)+CO2(g) △H=373.2kJ·mol-1,达到平衡后,为提高反应的速率和NO的转化率,采取的正确措施是
1/2N2(g)+CO2(g) △H=373.2kJ·mol-1,达到平衡后,为提高反应的速率和NO的转化率,采取的正确措施是
A. 加催化剂同时升高温度 B. 加催化剂同时增大压强
C. 升高温度同时充入N2 D. 降低温度同时减小压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中的一些问题常涉及化学知识,下列叙述正确的是
A. 过多食用糖类物质如淀粉等不会致人发胖
B. 棉花的主要成分是纤维素
C. 淀粉在人体内直接水解生成葡萄糖,供人体组织的所有营养需要
D. 纤维素在人体消化过程中起重要作用,纤维素可以作为人类的营养物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿抽出的废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO![]() 。某研究性学习小组获取这种废液来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
。某研究性学习小组获取这种废液来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
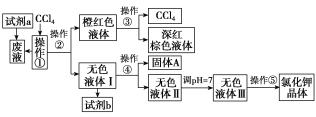
可供试剂a、b的选择试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2溶液、稀盐酸。(已知:2Br-+2H++H2O2=Br2+2H2O)
请根据以上流程,回答相关问题:
(1)试剂a应该选用_________________。
(2)操作①、②、③、④、⑤的名称是______________________________(填字母)。
A.萃取、过滤、分液、过滤、蒸发 B.萃取、分液、蒸馏、过滤、蒸发
C.分液、萃取、过滤、过滤、蒸发 D.萃取、分液、分液、过滤、蒸发
(3)除去无色液体Ⅰ中的Ca2+、Mg2+、SO![]() ,选出b所代表的试剂,按滴加顺序依次是______________(填化学式)。
,选出b所代表的试剂,按滴加顺序依次是______________(填化学式)。
(4)调节pH的作用是________________,操作方法是_________________。
(5)操作⑤中用到的瓷质仪器的名称是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下的甲烷和一氧化碳的混合气体8.96L,其质量为7.60g,求:
(1)混合气体的平均相对分子质量;
(2)混合气体中甲烷的体积;
(3)混合气体中一氧化碳的质量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com