


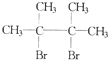
 ;A的结构简式为(CH3)2C═C(CH3)2;E的结构简式为
;A的结构简式为(CH3)2C═C(CH3)2;E的结构简式为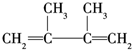 ;F1的结构简式为
;F1的结构简式为
 .
.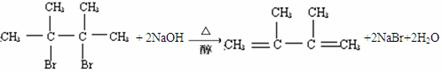 .
. 分析 烯烃A含有碳碳双键,与溴发生加成反应生成D为C6H12Br2,仪器分析显示D有四个完全对称的甲基,D是 ,可知A为(CH3)2C═C(CH3)2,A与HBr发生加成反应生成C为(CH3)2CBrCH(CH3)2,A与氢气发生加成反应生成B,B与溴发生取代反应生成C,则B为(CH3)2CHCH(CH3)2,D在足量的氢氧化钠醇溶液、加热条件下发生消去反应生成E,则E为
,可知A为(CH3)2C═C(CH3)2,A与HBr发生加成反应生成C为(CH3)2CBrCH(CH3)2,A与氢气发生加成反应生成B,B与溴发生取代反应生成C,则B为(CH3)2CHCH(CH3)2,D在足量的氢氧化钠醇溶液、加热条件下发生消去反应生成E,则E为 ,E与适量Br2反应时有两种加成方式,即1,2-加成生成
,E与适量Br2反应时有两种加成方式,即1,2-加成生成 和1,4-加成生成
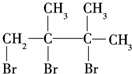
和1,4-加成生成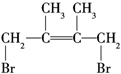 ,再加成HBr时F1有两种加成产物,F2只有一种加成产物,则F1为
,再加成HBr时F1有两种加成产物,F2只有一种加成产物,则F1为 ,F2为
,F2为 ,故G1为
,故G1为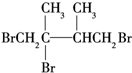 ,G2为
,G2为 ,据此解答.
,据此解答.
解答 解:烯烃A含有碳碳双键,与溴发生加成反应生成D为C6H12Br2,仪器分析显示D有四个完全对称的甲基,D是 ,可知A为(CH3)2C═C(CH3)2,A与HBr发生加成反应生成C为(CH3)2CBrCH(CH3)2,A与氢气发生加成反应生成B,B与溴发生取代反应生成C,则B为(CH3)2CHCH(CH3)2,D在足量的氢氧化钠醇溶液、加热条件下发生消去反应生成E,则E为
,可知A为(CH3)2C═C(CH3)2,A与HBr发生加成反应生成C为(CH3)2CBrCH(CH3)2,A与氢气发生加成反应生成B,B与溴发生取代反应生成C,则B为(CH3)2CHCH(CH3)2,D在足量的氢氧化钠醇溶液、加热条件下发生消去反应生成E,则E为 ,E与适量Br2反应时有两种加成方式,即1,2-加成生成
,E与适量Br2反应时有两种加成方式,即1,2-加成生成 和1,4-加成生成
和1,4-加成生成 ,再加成HBr时F1有两种加成产物,F2只有一种加成产物,则F1为
,再加成HBr时F1有两种加成产物,F2只有一种加成产物,则F1为 ,F2为
,F2为 ,故G1为
,故G1为 ,G2为
,G2为 .
.
(1)D的结构简式为  ;A的结构简式为(CH3)2C═C(CH3)2;E的结构简式为
;A的结构简式为(CH3)2C═C(CH3)2;E的结构简式为 ;F1的结构简式为
;F1的结构简式为  ,
,
故答案为: ;(CH3)2C═C(CH3)2;
;(CH3)2C═C(CH3)2; ;
; ;
;
(2)G2的结构简式是: ,故答案为:
,故答案为: ;
;
(3)反应⑤为 在氢氧化钠的醇溶液中发生消去反应,反应方程式为
在氢氧化钠的醇溶液中发生消去反应,反应方程式为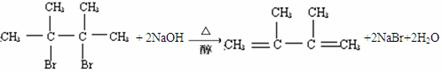 ,
,
故答案为: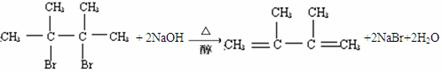 .
.
点评 本题考查有机物的推断,以D的分子式与结构特点为突破口,结合反应条件进行推断,需要学生熟练掌握官能团的性质与转化,易错点为F1和F2,G1和G2的推断,注意理解烯烃的1,2-加成与1,4-加成反应.


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1NaCl溶液中含有NA个Na+ | |
| B. | 25℃,101kPa,64gSO2中含有的原子数为3NA | |
| C. | 在常温常压下,22.4LCl2含有的分子数为NA | |
| D. | 标准状况下,11.2LCCl4含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯分子中,C、H原子个数比为1:2 | |
| B. | 乙烯易发生加成反应且1mol乙烯加成时只需1mol溴 | |
| C. | 乙烯能被氧化 | |
| D. | 乙烯完全燃烧生成等物质的量的CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何化学反应都能设计成原电池 | |
| B. | 原电池两极均发生还原反应 | |
| C. | 原电池中的阳离子向负极移动 | |
| D. | 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原混合溶液中c(K+)为2mol•L-1 | B. | 上述电解过程中共转移2mol电子 | ||
| C. | 电解得到铜的物质的量为0.5mol | D. | 电解后溶液中c(H+)为2mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol D2O所含质子数为12 NA | |
| B. | 1 mol C16H34中的极性键数为34 NA | |
| C. | 10 g 氖气所含原子数为NA | |
| D. | 22.4 L正戊烷含氢原子数为12 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
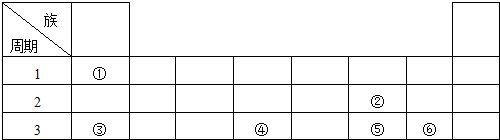
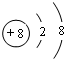 .
.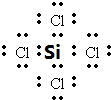 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
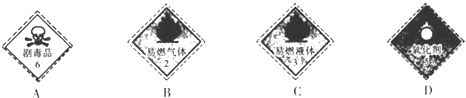
 .
. .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com