
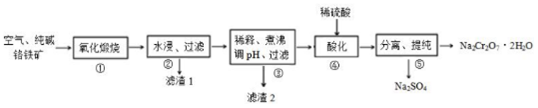
分析 铬铁矿在空气中与纯碱煅烧生成Na2CrO4和一种红棕色固体,同时释放出CO2气体,同时A12O3+Na2CO3 $\frac{\underline{\;高温\;}}{\;}$2NaAlO2+CO2↑,可知主反应为4Fe(CrO2)2+7O2+8Na2CO3$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2,铬铁矿在空气中与纯碱煅烧生成物通过水浸NaAlO2进入浸出液中,而不溶的Fe2O3形成滤渣1,浸出液通过除杂,通入CO2气体,形成滤渣2Al(OH)3沉淀,最后分离出Na2CrO4溶液,经过酸化、过滤、结晶得到最终产品重铬酸钠晶体( Na2Cr2O7•2H2O);
(1)根据化合物中正负化合价之和为0计算Cr的化合价;从影响反应速率的因素角度考虑;
(2)根据流程图可知,煅烧过程中,铬铁矿中的Al2O3与纯碱反应生成了CO2,然后依据元素守恒配平,得化学方程式;煅烧时铬铁矿的成分之一Fe2O3没有参与反应,也不溶解与水中,
(3)铬铁矿煅烧时生成的NaAlO2在水溶液中与CO2生成Al(OH)3沉淀;
(4)步骤④,向滤液中加入稀硫酸,溶液由黄色变为橙色,得到Na2Cr2O7和 Na2SO4的混合溶液,说明溶液中存在CrO42-在酸性条件下转化为Cr2O72-的过程,是非氧化还原反应,只需要根据电荷守恒和原子守恒即可写出此反应的离子方程式;
(5)在酸性条件下,Fe2+可以将Cr2O72-还原为Cr3+,根据电子守恒、电荷守恒和原子守恒即可写出此反应的离子方程式;根据溶度积常数Ksp=c(Cr3+)×c3(OH-)=1.0×10-32,先计算出,再计算溶液pH.
解答 解:铬铁矿在空气中与纯碱煅烧生成Na2CrO4和一种红棕色固体,同时释放出CO2气体,同时A12O3+Na2CO3 $\frac{\underline{\;高温\;}}{\;}$2NaAlO2+CO2↑,可知主反应为4Fe(CrO2)2+7O2+8Na2CO3$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2,铬铁矿在空气中与纯碱煅烧生成物通过水浸NaAlO2进入浸出液中,而不溶的Fe2O3形成滤渣1,浸出液通过除杂,通入CO2气体,形成滤渣2Al(OH)3沉淀,最后分离出Na2CrO4溶液,经过酸化、过滤、结晶得到最终产品重铬酸钠晶体( Na2Cr2O7•2H2O);
(1)Fe(CrO2)2中,Fe为+2价,+2+2[x+(-2)×2]=0,解得x=+3;化煅烧时将铬铁矿粉碎,增大接触面积,加快铬铁矿煅烧速率,
故答案为:+3;增大接触面积,加快铬铁矿煅烧速率;
(2)根据流程图可知,煅烧过程中,铬铁矿中的Al2O3与纯碱反应生成了CO2,然后依据元素守恒配平,得化学方程式为Al2O3+Na2CO3$\frac{\underline{\;高温\;}}{\;}$2NaAlO2+CO2↑;煅烧时铬铁矿的成分之一Fe2O3没有参与反应,也不溶解与水中,所以滤渣1的成分为Fe2O3,
故答案为:Al2O3+Na2CO3$\frac{\underline{\;高温\;}}{\;}$2NaAlO2+CO2↑;Fe2O3;
(3)铬铁矿煅烧时生成的NaAlO2在水溶液中与CO2生成Al(OH)3沉淀,故滤渣2的成分为Al(OH)3,故答案为:Al(OH)3;
(4)已知2H++2CrO42-?2H2O+Cr2O72-向滤液中加入稀硫酸,溶液由黄色变为橙色,说明平衡正向移动,发生反应的离子方程式为2H++2CrO42-=2H2O+Cr2O72-,故答案为:2H++2CrO42-=2H2O+Cr2O72-;
(5)在酸性条件下,Fe2+可以还原Cr2O72-为Cr3+,发生反应的离子方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;已知Ksp=c(Cr3+)×c3(OH-)=1.0×10-32、c(Cr3+)=10-5mol/L,则c(OH-)=1.0×10-9mol/L,则c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$=$\frac{1×1{0}^{-14}}{{10}^{-9}}$mol/L=10-5mol/L,则溶液的pH=5,
故答案为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;5.
点评 作为工业流程题,本题思路比较清晰,涉及反应原理分析、实验的基本操作及溶液的pH计算,题项设置简单,综合程度较高,同时考查学生分析问题和解决问题能力,难度中等.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | Na与Na2SO4在灼烧时火焰颜色相同 | |
| B. | 焰色反应实验中常用稀盐酸洗涤金属丝 | |
| C. | 可以用焰色反应来区别NaCl和KCl | |
| D. | 观察K2CO3的焰色应透过红色的玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盛放NaOH溶液的试剂瓶用磨口玻璃塞 | |
| B. | 氢氟酸保存在塑料瓶中 | |
| C. | 过氧化钠保存在广口瓶中 | |
| D. | 浓盐酸保存在细口试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
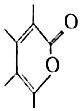 以下说法正确的是( )
以下说法正确的是( )| A. | 一Me基团的电子式为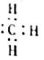 | |
| B. | 该合成过程的反应类型属于加成反应 | |
| C. | 产物与 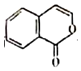 互为同分异构体 互为同分异构体 | |
| D. | 产物可与H2发生加成反应,反应的物质的量之比为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m=2 | |
| B. | 两次平衡的平衡常数相同 | |
| C. | X与Y平衡转化率之比为1:1 | |
| D. | 第二次平衡时,Z的浓度为0.4mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
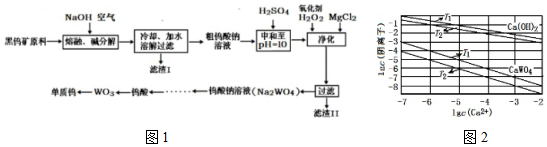
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成分 | WO3 W2O5 WO2 W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
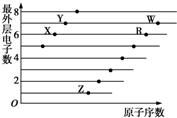 如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )
如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )| A. | X与W形成的化合物中只有共价键 | B. | X与Z形成的化合物中只有离子键 | ||
| C. | 元素的非金属性:X>R>W | D. | 简单离子的半径:W>R>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20mx | B. | 20x/m | C. | 25mx | D. | 50m/x |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com