
【题目】E是一种能发生加聚反应的有机合成中间体,合成E的路线如下。

(1)反应①的类型是________________;反应②的试剂和条件是__________________。
(2)写出反应③的化学方程式_______________________________。
(3)D的结构简式___________。
D有多种同分异构体,写出一种符合下列要求的结构简式____________。
i. 含有苯环 ii. 能发生水解反应 iii. 苯环上的一溴代物有两种
(4)通过反应⑤得到E的产率不高,原因是___________________________。
(5)设计一条由CH3CH=CHCH3为原料制备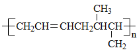 的合成路线。___________
的合成路线。___________
(合成路线常用的表示方法为:X![]() Y……
Y……![]() 目标产物)
目标产物)
【答案】加成 NaOH/H2O、加热 ![]()
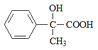
![]() D既有羟基又有羧基,在浓硫酸作用下发生消去反应时,会生成酯类等副产物,影响产率
D既有羟基又有羧基,在浓硫酸作用下发生消去反应时,会生成酯类等副产物,影响产率 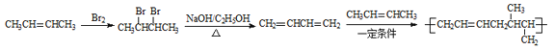
【解析】
由B物质逆向推断可知,A为苯乙烯,与Br2发生加成反应得到B,以物质D为中心,正向和逆向推断可知,D中一定含有羟基和羧基,C物质被两次氧化得到D,可知C物质中含有羟基,由此继续逆向推断可知,B物质中的Br原子水解得到羟基,再被氧化得到羧基,E物质是D物质自身酯化得到的酯;
(1)依据上述推断分析可知,A为苯乙烯,与Br2发生加成反应得到B,则反应①是加成反应,反应②是卤代烃的水解反应,反应条件为氢氧化钠的水溶液、加热,
故答案为:加成;NaOH/H2O、加热;
(2)反应③是C物质中的羟基被氧化成醛基,化学反应方程式为:![]() ,
,
故答案为:![]() ;
;
(3)由物质B可知,D 中含有一个苯环,另3个C原子相连,其中D含有一个羟基和一个羧基,即可推断出D的结构简式为: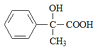 ,若D的同分异构体含有苯环且能发生水解反应即含有酯基,并且苯环上的一溴代物有两种,可推断出D的同分异构体的结构简式为:
,若D的同分异构体含有苯环且能发生水解反应即含有酯基,并且苯环上的一溴代物有两种,可推断出D的同分异构体的结构简式为:![]() ,
,
故答案为: ;
;![]() ;
;
(4)通过反应⑤得到E的产率不高,是由于D既有羟基又有羧基,在浓硫酸作用下发生消去反应时,会生成酯类等副产物,影响产率,
故答案为:D既有羟基又有羧基,在浓硫酸作用下发生消去反应时,会生成酯类等副产物,影响产率;
(5)由聚合物的结构逆向推断形成聚合物的单体是2-丁烯和1,3丁二烯,所以只要用2-丁烯合成出1,3丁二烯再发生加聚反应即可,合成路线为: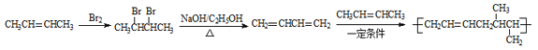 ,
,
故答案为: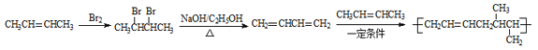 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。电解一段时间后,若在电解池中C极一侧出来的气体无色无味,D极一侧出来的气体呈黄绿色有刺激性气味。请回答以下问题:

(1)已知铅蓄电池在放电时发生的反应:Pb+PbO2+4H++2SO42-=2PbSO4+2H2O,则A极的电极反应为___________________________;
(2)电解饱和食盐水的离子反应方程式是__________________;
(3)电极C的电极反应是_____________________________________________;
(4)电解时为防止两种气体产物混合,用阳离子交换膜做隔膜。则电解时Na+从______极区移向_____极区(填“C”或“D”);
(5)若电路上有0.2mol电子的电量通过,则铅蓄电池中消耗硫酸_________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行以下可逆反应:M(g)+N(g)![]() P(g)+2L在不同的条件下P的百分含量P %的变化情况如下图,则该反应( )
P(g)+2L在不同的条件下P的百分含量P %的变化情况如下图,则该反应( )

A. 正反应放热,L是固体
B. 正反应放热,L是气体
C. 正反应吸热,L是气体
D. 正反应放热,L是固体或气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最活泼的金属元素、最活泼的非金属元素、常温下呈液态的金属(价电子排布为5d106s2)元素分别位于下面元素周期表中的( )

A. s区、p区、ds区 B. s区、p区、d区
C. f区、p区、ds区 D. s区、f区、ds区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)钒在元素周期表中的位置为__________,其价层电子排布图为____________。
(2)基态镓(Ga)原子的电子排布式:__________________。
(3) Fe3+的电子排布式为__________________。
(4)基态铜原子的核外电子排布式为__________________。
(5) Ni2+的价层电子排布图为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. KClO 碱性溶液与 Fe(OH)3 反应:3ClO+2Fe(OH)3=2FeO42+3Cl+4H++H2O
B. 用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠:S2O32- +2H+= SO2↑+S↓+H2O
C. 硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH![]() C17H35COOC2H5+H218O
C17H35COOC2H5+H218O
D. 向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,BaSO4饱和溶液中加少量的BaCl2溶液产生BaSO4沉淀,若以Ksp表示该温度下BaSO4的溶度积常数,则平衡后的溶液中
A. c(Ba2+)=c(SO42-)=![]() B. c(Ba2+)·c(SO42-)>Ksp,c(Ba2+)=c(SO42-)
B. c(Ba2+)·c(SO42-)>Ksp,c(Ba2+)=c(SO42-)
C. c(Ba2+)·c(SO42-)=Ksp,c(Ba2+)>c(SO42-) D. c(Ba2+)·c(SO42-)≠Ksp,c(Ba2+)<c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000mol/L NaOH溶液滴定 20.00mL 0.1000 mol/L
CH3COOH溶液滴定曲线如右图。下列说法正确的是

A. 点①所示溶液中:c(CH3COO-)+ c(OH-) =c(CH3COOH)+ c(H+)
B. 点②所示溶液中:c(Na+) =c(CH3COOH)+ c(CH3COO-)
C. 点③所示溶液中:c(Na+)> c(OH-)> c(CH3COO-)> c(H+)
D. 滴定过程中可能出现:c(CH3COOH)> c(CH3COO-)> c(H+)> c(Na+)> c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.向蒸馏水中滴加浓H2SO4时,KW不变
B.常温下,0.005mol·L-1Ba(OH)2溶液pH为12
C.Na2CO3水解的离子方程式为:CO32- + 2H2O![]() H2CO3 + 2OH-
H2CO3 + 2OH-
D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com