
”¾ĢāÄæ”æ£Ø1£©AŗĶB·“Ӧɜ³ÉC£¬¼Ł¶Ø·“Ó¦øÕæŖŹ¼Ö»ÓŠA”¢B£¬ĖüĆĒµÄĘšŹ¼ÅØ¶Č¾łĪŖ1mol/L”£·“Ó¦½ųŠŠ2minŗóAµÄÅضČĪŖ0.8mol/L£¬BµÄÅضČĪŖ0.6mol/L£¬CµÄÅضČĪŖ0.6mol/L”£ŌņŌŚÕā2 minÄŚ·“Ó¦µÄĘ½¾łĖŁĀŹVA =_______ mol/(L”¤ min)£¬VB =________ mol/(L”¤ min)£¬øĆ·“Ó¦2 minÄŚA”¢B”¢CČżÖÖĪļÖŹµÄ»Æѧ·“Ó¦ĖŁĀŹÖ®±ČĪŖ:________________________”£
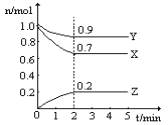
£Ø2£©Ä³ĪĀ¶ČŹ±£¬ŌŚŅ»øö2LµÄĆܱÕČŻĘ÷ÖŠ£¬X”¢Y”¢ZČżÖÖĪļÖŹµÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆĒśĻßČēÉĻĶ¼ĖłŹ¾”£øł¾ŻĶ¼ÖŠŹż¾Ż£¬ŹŌĢīŠ“ĻĀĮŠæÕ°×£ŗ
¢ŁøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ__________________________________________________£»
¢Ś“ÓæŖŹ¼ÖĮ2min£¬ZµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ______________________”£
”¾“š°ø”æ 0.1 0.2 1 £ŗ2 £ŗ3 3X+Y![]() 2Z 0.05mol/(L”¤min)
2Z 0.05mol/(L”¤min)
”¾½āĪö”æ£Ø1£©øł¾Ż·“Ó¦ĖŁĀŹŹĒµ„Ī»Ź±¼äÄŚÅØ¶ČµÄ±ä»ÆĮæ·ÖĪö¼ĘĖć£»
£Ø2£©øł¾ŻĪļÖŹµÄ±ä»ÆÅŠ¶Ļ·“Ó¦ĪļŗĶÉś³ÉĪļ£¬øł¾Ż·“Ó¦ĖŁĀŹŹĒµ„Ī»Ź±¼äÄŚÅØ¶ČµÄ±ä»ÆĮæ¼ĘĖć”£
£Ø1£©AŗĶB·“Ӧɜ³ÉC£¬¼Ł¶Ø·“Ó¦øÕæŖŹ¼Ö»ÓŠA”¢B£¬ĖüĆĒµÄĘšŹ¼ÅØ¶Č¾łĪŖ1mol/L”£·“Ó¦½ųŠŠ2minŗóAµÄÅضČĪŖ0.8mol/L£¬BµÄÅضČĪŖ0.6mol/L£¬CµÄÅضČĪŖ0.6mol/L”£ŌņŌŚÕā2 minÄŚ·“Ó¦µÄĘ½¾łĖŁĀŹVA=£Ø1mol/L£0.8mol/L£©”Ā2min=0.1 mol/(L”¤min)£¬VB=£Ø1mol/L£0.6mol/L£©”Ā2min=0.2 mol/(L”¤min)”£·“Ó¦ĖŁĀŹÖ®±ČŹĒĻąĶ¬Ź±¼äÄŚÅØ¶ČµÄ±ä»ÆĮæÖ®±Č£¬øĆ·“Ó¦2 minÄŚA”¢B”¢CČżÖÖĪļÖŹµÄ»Æѧ·“Ó¦ĖŁĀŹÖ®±ČĪŖ0.2£ŗ0.4£ŗ0.6£½1£ŗ2£ŗ3”£
£Ø2£©¢Łøł¾ŻĶ¼ĻńæÉÖŖxÓėyµÄĪļÖŹµÄĮæ¼õÉŁ£¬ŹĒ·“Ó¦Īļ£¬zŹĒÉś³ÉĪļ£¬2minŹ±·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬“ĖŹ±x¼õÉŁ0.3mol£¬y¼õÉŁ0.1mol£¬zŌö¼Ó0.2mol£¬Ņņ“Ėøł¾Ż±ä»ÆĮæÖ®±ČŹĒ»Æѧ¼ĘĮæŹżÖ®±ČæÉÖŖøĆ·“Ó¦µÄ·½³ĢŹ½ĪŖ3X+Y![]() 2Z£»
2Z£»
¢Ś“ÓæŖŹ¼ÖĮ2min£¬ZµÄÅØ¶Č±ä»ÆĮæŹĒ0.2mol”Ā2L£½0.1mol/L£¬ĖłŅŌĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.1mol/L”Ā2min£½0.05mol/(L”¤min)”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ“߻ƻ¹ŌCO2ŹĒ½ā¾öĪĀŹŅŠ§Ó¦¼°ÄÜŌ“ĪŹĢāµÄÖŲŅŖŹÖ¶ĪÖ®Ņ»”£ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ£¬CO2ŗĶH2ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ó¦£ŗCO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g)”£CO2”¢H2”¢CH3OH”¢H2OµÄÅØ¶Č¾ł²»ŌŁøı䏱£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
CH3OH(g) + H2O(g)”£CO2”¢H2”¢CH3OH”¢H2OµÄÅØ¶Č¾ł²»ŌŁøı䏱£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. CO2”¢H2”¢CH3OH”¢H2OµÄÅضČŅ»¶ØĻąµČ
B. øĆ·“Ó¦ŅŃ¾“ļµ½»ÆŃ§Ę½ŗāדĢ¬
C. CO2ŗĶH2ĶźČ«×Ŗ»ÆĪŖCH3OHŗĶH2O
D. CO2”¢H2µÄ·“Ó¦ĖŁĀŹµČÓŚCH3OH”¢H2OµÄ·“Ó¦ĖŁĀŹĒŅĪŖĮć
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŽĖ®MgBr2 æɹć·ŗÓĆÓŚÓŠ»ś·“Ó¦“߻ƼĮ”¢ĪŪĖ®“¦Ąķ¼ĮµČ”£ŹµŃéŹŅæÉÓĆĆ¾Š¼ÓėŅŗäåĪŖŌĮĻ£¬²ÉÓĆĻĀĶ¼×°ÖĆÖʱøĪŽĖ®MgBr2,Ēė»Ų“š:
£Ø1£©Ź¶±šĻĀĶ¼ÖŠŅĒĘ÷”£AµÄĆū³ĘŹĒ______£¬BŹĒ_______
£Ø2£©ŹµŃ鏱£¬æÉĻņ×°ÖĆCÖŠ»ŗĀżĶØČėøÉŌļµÄµŖĘų£¬Ö±ÖĮäåĶźČ«µ¼ČėČż¾±ĘæÖŠ”£øÉŌļµÄµŖĘųÄܽ«Ņŗä哵³ö£¬ŅņĪŖŅŗäå¾ßÓŠ________µÄŠŌÖŹ;ŹµŃéÖŠ²»ÄÜÓĆøÉŌļæÕĘų“śĢęøÉŌļN2£¬ŌŅņŹĒ£ŗ___________________________________________________________

£Ø3£©ŅŃÖŖ:MgŗĶBr2·“Ó¦¾ēĮŅ·ÅČČ;ŅŅĆŃ(C2H5OC2H5)¼«Ņ×»Ó·¢”£MgBr2ŗĶŅŅĆŃÄÜ·¢ÉśČēĻĀ·“Ó¦:MgBr2+3C2H5OC2H5![]() MgBr2”¤3C2H5OC2H5+Q(Q>0);·“Ó¦Ķź±Ļŗó»Öø“ÖĮŹŅĪĀ£¬¹żĀĖ£¬ĀĖŅŗ×ŖŅĘÖĮĮķŅ»øÉŌļµÄÉÕĘæÖŠ£¬ĄäČ“ÖĮ0”ćC,Īö³ö¾§Ģ壬ŌŁ¹żĀĖµĆČżŅŅĆŃŗĻäå»ÆĆ¾“ÖĘ·”£µŚŅ»“Ī¹żĀĖ³żČ„µÄĪļÖŹŹĒ_______”£¹żĀĖ±ŲŠėÓƵ½µÄ²£Į§ŅĒĘ÷ŹĒ:_______”£
MgBr2”¤3C2H5OC2H5+Q(Q>0);·“Ó¦Ķź±Ļŗó»Öø“ÖĮŹŅĪĀ£¬¹żĀĖ£¬ĀĖŅŗ×ŖŅĘÖĮĮķŅ»øÉŌļµÄÉÕĘæÖŠ£¬ĄäČ“ÖĮ0”ćC,Īö³ö¾§Ģ壬ŌŁ¹żĀĖµĆČżŅŅĆŃŗĻäå»ÆĆ¾“ÖĘ·”£µŚŅ»“Ī¹żĀĖ³żČ„µÄĪļÖŹŹĒ_______”£¹żĀĖ±ŲŠėÓƵ½µÄ²£Į§ŅĒĘ÷ŹĒ:_______”£
£Ø4£©ŹŌÓĆĘ½ŗāŅĘ¶ÆµÄŌĄķĖµĆ÷µĆµ½ČżŅŅĆŃŗĻäå»ÆĆ¾ŗ󣬼ÓČČÓŠĄūÓŚĘä·Ö½ā£¬µĆĪŽĖ®MgBr2²śĘ·µÄŌŅņ: ______________________________
£Ø5£©ĪŖ²ā¶Ø²śĘ·µÄ“æ¶Č£¬æÉÓĆEDTA(¼ņŠ“ĪŖY4-)±ź×¼ČÜŅŗµĪ¶Ø£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½:Mg2++Y4-====Mg Y2-
¢ŁµĪ¶ØĒ°ČóĻ“µĪ¶Ø¹ÜµÄ²Ł×÷·½·ØŹĒ____________________________
¢Ś²ā¶ØĒ°£¬ĻČ³ĘČ”0.2500gĪŽĖ®MgBr2²śĘ·£¬Čܽāŗó£¬ÓĆ0.0500mol/LµÄEDTA ±ź×¼ČÜŅŗµĪ¶ØÖĮÖÕµć£¬ĻūŗÄEDTA ±ź×¼ČÜŅŗ26.50mL,Ōņ²āµĆĪŽĖ®MgBr2²śĘ·µÄ“æ¶ČŹĒ___________ (ŅŌÖŹĮæ·ÖŹż±ķŹ¾)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ½«NaOHČÜŅŗµĪ¼Óµ½H2XČÜŅŗÖŠ£¬»ģŗĻČÜŅŗµÄpHÓė![]() ”¢
”¢![]() µÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
µÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ

A. H2XĪŖ¶žŌŖĒæĖį
B. µ±![]() =1Ź±£¬ČÜŅŗÖŠc(HX”„)=c(H2X)
=1Ź±£¬ČÜŅŗÖŠc(HX”„)=c(H2X)
C. NaHXČÜŅŗÖŠc(H+)<c(OH”„)
D. µ±ČÜŅŗpH=4.6Ź±c(HX”„)>c (X2-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪåĖ®ĮņĖįĶ(CuSO4”¤5H2O)ŗĶĮłĖ®ĮņĖįŃĒĢśļ§[(NH4)2Fe(SO4)2”¤6H2O]¶¼ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ÓĆĶ¾Ź®·Ö¹ć·ŗ”£
Ēė»Ų“šÓėÕāĮ½ÖÖĪļÖŹÖŠŌŖĖŲÓŠ¹ŲµÄŅ»Š©ĪŹĢā”£
£Ø1£©»łĢ¬ĢśŌ×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ_______£»»łĢ¬ĶŌ×ӵĵē×ÓÕ¼¾ŻµÄ×īøßÄܲć·ūŗÅĪŖ_______ ”£
£Ø2£©ŃõŌŖĖŲµÄµŚŅ»µēĄėÄÜŠ”ÓŚµŖŌŖĖŲ£¬ĘäŌŅņŹĒ_______ ”£
£Ø3£©SO42-”¢H2O”¢NH4+ČżÖÖĪ¢Į£ÖŠ£¬æռ乹ŠĶĪŖÕżĖÄĆęĢåµÄŹĒ_______£»NH4+ÖŠµŖŌ×ÓµÄŌӻƹģµĄĄąŠĶŹĒ_______”£
£Ø4£©Š“³öÓėSO42-»„ĪŖµČµē×ÓĢåµÄ·Ö×ӵĻÆѧŹ½_______ (Š“Ņ»ÖÖ)”£
£Ø5£©CuÓėAuµÄŗĻ½šæÉŠĪ³ÉĆęŠÄĮ¢·½×īĆܶѻżµÄ¾§Ģ壬ŌŚøĆ¾§°ūÖŠCuŌ×Ó“¦ÓŚĆęŠÄ£¬øĆ¾§Ģå¾ßÓŠ“¢Ēā¹¦ÄÜ£¬ĒāŌ×ÓæɽųČėµ½CuŌ×ÓÓėAuŌ×Ó¹¹³ÉµÄĮ¢·½ĢåæÕĻ¶ÖŠ£¬“¢ĒāŗóµÄ¾§°ū½į¹¹Óė½šøÕŹÆ¾§°ū½į¹¹(ČēĶ¼)ĻąĖĘ£¬øĆ¾§Ģå“¢ĒāŗóµÄ»ÆѧŹ½ĪŖ_______£¬ČōøĆ¾§ĢåµÄĆܶČĪŖ¦Ńg.cm-3£¬Ōņ¾§°ūÖŠCuŌ×ÓÓėAuŌ×ÓÖŠŠÄµÄ×ī¶Ģ¾ąĄėd=_______cm(NA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ)”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æX”¢Y”¢ZŗĶW“ś±ķŌ×ÓŠņŹżŅĄŅūŌö“óµÄĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬XŌ×ÓŗĖČƻӊ֊×Ó£¬ŌŚÖÜĘŚ±ķÖŠ£¬ZÓėY”¢W¾łĻąĮŚ£» Y”¢ZŗĶWµÄŌ×Ó×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ17”£ŌņĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
A. Y”¢ZŗĶWæÉÄÜĪ»ÓŚĶ¬Ņ»ÖÜĘŚ
B. YŗĶW·Ö±šŠĪ³ÉµÄŗ¬ŃõĖį¾łĪŖĒæĖį
C. Y”¢Z”¢W·Ö±šŠĪ³ÉµÄ¼ņµ„Ēā»ÆĪļÖŠ£¬WµÄ¼ņµ„Ēā»ÆĪļĻą¶Ō·Ö×ÓÖŹĮæ×ī“ó£¬ČŪ·šµć×īøß
D. X”¢Y”¢ZŗĶWæÉŅŌ×é³ÉŌ×ÓøöŹż±ČĪŖ5: 1:4:1µÄĄė×Ó»ÆŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æC”¢NŗĶSiÄÜŠĪ³É¶ąÖÖøßÓ²¶Č²ÄĮĻ£¬ČēSi3N4,C3N4,SiC.
(1)Si3N4ŗĶC3N4ÖŠÓ²¶Č½ĻøߵďĒ______,ĄķÓÉŹĒ_________.
(2)CŗĶNÄÜŠĪ³ÉŅ»ÖÖĄąŹÆÄ«½į¹¹²ÄĮĻ£¬ĘäŗĻ³É¹ż³ĢČēĻĀĶ¼ĖłŹ¾”£øĆĄąŹÆÄ«½į¹¹²ÄĮĻ»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖ_________”£ĘäŗĻ³É¹ż³ĢÖŠÓŠČż¾ŪĒč°·ŠĪ³É£¬Čż¾ŪĒč°·ÖŠNŌ×ÓµÄŌӻƷ½Ź½ÓŠ_____________”£

(3)CŗĶN»¹ÄÜŠĪ³ÉŅ»ÖÖĪåŌŖ»·×“ÓŠ»śĪļßäßņ(im)£¬Ęä½į¹¹ĪŖ![]() ”£»ÆŗĻĪļ[Co(im)6]SiF6µÄ½į¹¹Ź¾ŅāĶ¼ČēĻĀ:
”£»ÆŗĻĪļ[Co(im)6]SiF6µÄ½į¹¹Ź¾ŅāĶ¼ČēĻĀ:
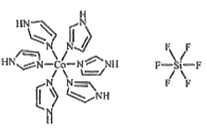
¢ŁCoŌ×ӵļŪ²ćµē×Ó¹ģµĄ±ķ“ļŹ½(¼Ū²ćµē×ÓÅŲ¼Ķ¼)ĪŖ_____”£NÓėCoÖ®¼äµÄ»Æѧ¼üĄąŠĶŹĒ___£¬ÅŠ¶ĻµÄĄķÓÉŹĒ__________”£
¢ŚŅõĄė×ÓSiF62-ÖŠŠÄŌ×ÓSiµÄ¼Ū²ćµē×Ó¶ŌŹżĪŖ______”£ŃōĄė×Ó(Co(im)6]2+ŗĶSiF62-Ö®¼ä³żĮĖŅõŃōĄė×Ó¼äµÄ¾²µē×÷ÓĆĮ¦£¬»¹“ęŌŚĒā¼ü×÷ÓĆ£¬»³öøĆĒā¼üµÄ±ķŹ¾Ź½_______”£
ĄżČēĖ®ÖŠĒā¼üµÄ±ķŹ¾Ź½ĪŖ: ![]()
(4)SiCĪŖĮ¢·½¾§Ļµ¾§Ģ壬¾§°ū ¢ŹżĪŖa,ŅŃÖŖSiŌ×Ó°ė¾¶ĪŖrSi,CŌ×Ó°ė¾¶ĪŖrC,øĆ¾§°ūÖŠŌ×ӵķ֏ż×ų±źĪŖ:

ŌņSiCĮ¢·½¾§°ūÖŠŗ¬ÓŠ____øöSiŌ×Ó”¢____øöCŌ×Ó£¬øĆ¾§°ūÖŠŌ×ÓµÄĢå»żÕ¼¾§°ūĢå»żµÄ°Ł·ÖĀŹĪŖ__________(ĮŠ³ö¼ĘĖćŹ½¼“æÉ)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚt”ꏱ£¬AgBrŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£®ÓÖÖŖt”ꏱAgClµÄKsp=4”Į10©10 £¬ ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£© 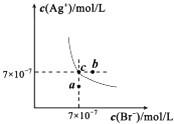
A.ŌŚt”ꏱ£¬AgBrµÄKspĪŖ4.9”Įl0©13
B.ŌŚAgBr±„ŗĶČÜŅŗÖŠ¼ÓČėNaBr¹ĢĢ壬æÉŹ¹ČÜŅŗÓÉcµćµ½bµć
C.Ķ¼ÖŠaµć¶ŌÓ¦µÄŹĒAgBrµÄ²»±„ŗĶČÜŅŗ
D.ŌŚt”ꏱ£¬AgCl£Øs£©+Br©£Øaq£©AgBr£Øs£©+Cl©£Øaq£©Ę½ŗā³£ŹżK”Ö816
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚĻø°ūÖ÷ŅŖ»Æѧ³É·ÖµÄŠšŹöÖŠ£¬²»ÕżČ·µÄŹĒ £Ø””””£©
A. ¶ÆĪļČéÖÖŠµÄČéĢĒŗĶÖ²ĪļĻø°ūÖŠµÄĻĖĪ¬ĖŲ¶¼ŹōÓŚ¶ąĢĒ
B. µØ¹Ģ“¼”¢Ī¬ÉśĖŲD¶¼ŹōÓŚÖ¬ÖŹ
C. ĶŃŃõŗĖĢĒŗĖĖįŹĒČ¾É«ĢåµÄÖ÷ŅŖ³É·ÖÖ®Ņ»
D. µ°°×ÖŹµÄ¶ąŃłŠŌÓė°±»łĖįµÄÖÖĄą”¢ŹżÄæŗĶÅÅĮŠĖ³ŠņµČÓŠ¹Ų
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com