
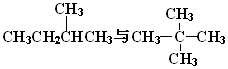 G£®
G£®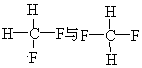
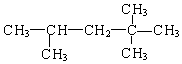 £¬ĖüŹĒĘūÓĶČ¼ÉÕĘ·ÖŹæ¹ÕšŠŌÄܵIJĪÕÕĪļ£¬ĘäÖŠAµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬ĒāŌ×ÓÖÖĄą×īÉŁµÄŅ»ÖÖ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬ĖüŹĒĘūÓĶČ¼ÉÕĘ·ÖŹæ¹ÕšŠŌÄܵIJĪÕÕĪļ£¬ĘäÖŠAµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬ĒāŌ×ÓÖÖĄą×īÉŁµÄŅ»ÖÖ½į¹¹¼ņŹ½ĪŖ£ŗ £»ČōAŹĒÓÉĻ©ĢžŗĶH2Ķعż¼Ó³É·“Ó¦µĆµ½£¬Š“³öøĆĻ©ĢžµÄĖłÓŠæÉÄܵĽį¹¹¼ņŹ½
£»ČōAŹĒÓÉĻ©ĢžŗĶH2Ķعż¼Ó³É·“Ó¦µĆµ½£¬Š“³öøĆĻ©ĢžµÄĖłÓŠæÉÄܵĽį¹¹¼ņŹ½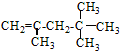 ”¢
”¢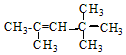 £®
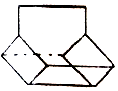
£®
·ÖĪö £Ø1£©Ķ¬Ī»ĖŲ£ŗÖŹ×ÓŹżĻąĶ¬£¬ÖŠ×ÓŹż²»Ķ¬µÄĶ¬Ņ»ŌŖĖŲ»„³ĘĶ¬Ī»ĖŲ£¬±ŲŠėŹĒŌŖĖŲµÄŌ×Ó£»Ķ¬ĻµĪļ£ŗ½į¹¹ĻąĖĘ£¬ŌŚ·Ö×Ó×é³ÉÉĻĻą²īŅ»øö»ņČōøÉøöCH 2Ō×ÓĶŵĻÆŗĻĪļ£¬±ŲŠėŹĒ»ÆŗĻĪļ£»
Ķ¬·ÖŅģ¹¹Ģå£ŗ·Ö×ÓŹ½ĻąĶ¬½į¹¹Ź½²»Ķ¬µÄ»ÆŗĻĪļ»„³ĘĶ¬·ÖŅģ¹¹Ģ壬±ŲŠėŹĒ»ÆŗĻĪļ£»Ķ¬ĖŲŅģŠĪĢå£ŗÓÉĶ¬ÖÖŌŖĖŲŠĪ³ÉµÄ²»Ķ¬µ„ÖŹ£¬ŹĒµ„ÖŹ£®Ķ¬Ņ»ĪļÖŹ£ŗĶźČ«ĻąĶ¬µÄĪļÖŹ£®
£Ø2£©AµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬µČŠ§ĒāŌ×ÓÖÖĄą×īÉŁµÄŅ»ÖÖĪļÖŹĪŖ2£¬2£¬3£¬3-Ėļ׻ł¶”Ķ飻½įŗĻĢ¼Ō×ÓŠĪ³É4øö¹²¼Ū¼üÅŠ¶ĻĻ©Ģž£»
£Ø3£©¢Ł½»µćĪŖĢ¼Ō×Ó£¬ÓĆHŌ×Ó±„ŗĶĢ¼µÄĖļŪ½į¹¹£¬¾Ż“ĖÅŠ¶ĻC”¢HŌ×ÓŹżÄ棬ŹéŠ“·Ö×ÓŹ½£»
¢Śøł¾ŻµČŠ§ĒāÅŠ¶ĻŅ»ĀČ“śĪļŹżÄ森
½ā“š ½ā£ŗA£®½šøÕŹÆÓėŹÆÄ«¾łĪŖĢ¼ŌŖĖŲŠĪ³ÉµÄ²»Ķ¬ÖÖµ„ÖŹ£¬»„ĪŖĶ¬ĖŲŅģŠĪĢ壻
B£®µķ·ŪÓėĻĖĪ¬ĖŲ¾łŹōÓŚøß·Ö×Ó»ÆŗĻĪļ£¬²»“ęŌŚŅŌÉĻ¹ŲĻµ£»
C£®ėÓėė®ÖŹ×ÓŹżĻąĶ¬£¬ÖŠ×ÓŹż²»Ķ¬£¬ŹōÓŚĶ¬Ī»ĖŲ£»
D£®¼×ĶéÓėĪģĶé½į¹¹ĻąĖĘ£¬·Ö×Ó×é³ÉÉĻĻą²ī4øöCH2Ō×ÓĶÅ£¬ŹōÓŚĶ¬ĻµĪļ£»
E£®ĘĻĢŃäēÓė¹ūĢĒ·Ö×ÓŹ½ĻąĶ¬£¬½į¹¹²»Ķ¬£¬ŹōÓŚĶ¬·ÖŅģ¹¹Ģ壻
F£®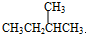 Óė
Óė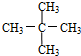 ·Ö×ÓŹ½ĻąĶ¬£¬½į¹¹²»Ķ¬£¬ŹōÓŚĶ¬·ÖŅģ¹¹Ģ壻
·Ö×ÓŹ½ĻąĶ¬£¬½į¹¹²»Ķ¬£¬ŹōÓŚĶ¬·ÖŅģ¹¹Ģ壻
G£®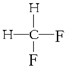 Óė
Óė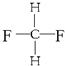 ŹōÓŚĶ¬ÖÖĪļÖŹ£»
ŹōÓŚĶ¬ÖÖĪļÖŹ£»
¹Ź“š°øĪŖ£ŗC£»D£»EF£»G£»
£Ø2£©AµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬µČŠ§ĒāŌ×ÓÖÖĄą×īÉŁµÄŅ»ÖÖĪļÖŹĪŖ2£¬2£¬3£¬3-Ėļ׻ł¶”Ķ飬½į¹¹¼ņŹ½ĪŖ£ŗ £¬ČōAŹĒÓÉĻ©ĢžŗĶH2Ķعż¼Ó³É·“Ó¦µĆµ½£¬ŌņøĆĻ©ĢžµÄ½į¹¹¼ņŹ½æÉÄÜĪŖ
£¬ČōAŹĒÓÉĻ©ĢžŗĶH2Ķعż¼Ó³É·“Ó¦µĆµ½£¬ŌņøĆĻ©ĢžµÄ½į¹¹¼ņŹ½æÉÄÜĪŖ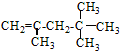 ”¢
”¢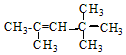 £»
£»
¹Ź“š°øĪŖ£ŗ £»
£»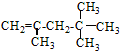 ”¢
”¢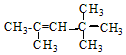 £»
£»
£Ø3£©¢Ł½»µćĪŖĢ¼Ō×Ó£¬ÓĆHŌ×Ó±„ŗĶĢ¼µÄĖļŪ½į¹¹£¬ÓÉĄ¶ĶéµÄ½į¹¹æÉÖŖ£¬·Ö×ÓÖŠŗ¬ÓŠ10øöCŌ×Ó”¢12øöHŌ×Ó£¬·Ö×ÓŹ½ĪŖC10H12£¬
¹Ź“š°øĪŖ£ŗC10H12£»
¢ŚøĆÓŠ»śĪļ·Ö×ÓŹōÓŚø߶ȶŌ³Ę½į¹¹£¬ÓŠČēĶ¼ĖłŹ¾£ŗ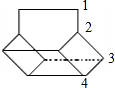 µÄ4ÖÖHŌ×Ó£¬ŌņĘäŅ»ĀČ“śĪļÓŠ4ÖÖ£¬¹Ź“š°øĪŖ£ŗ4£®
µÄ4ÖÖHŌ×Ó£¬ŌņĘäŅ»ĀČ“śĪļÓŠ4ÖÖ£¬¹Ź“š°øĪŖ£ŗ4£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ·ÖĄą”¢ÓŠ»śĪļµÄ½į¹¹ŗĶŠŌÖŹ”¢Ķ¬·ÖŅģ¹¹Ģ壬²ąÖŲӌѧɜµÄĖ«»łµÄ漲飬£Ø3£©ÖŠ×¢ŅāĄūÓĆÅŠ¶ĻµČŠ§HŌ×ÓÅŠ¶ĻŅ»ĀČ“śĪļĶ¬·ÖŅģ¹¹ĢåŹżÄ棬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ¼× | 1000mL 0.1mol/L HCOONaČÜŅŗ |
| ŅŅ | 1000mL 0.1mol/L CH3COONaČÜŅŗ |
| ±ū | 1000mLŗ¬HCOONa”¢CH3COONaø÷0.05molµÄČÜŅŗ |
| A£® | ČÜŅŗÖŠc£ØNa+£©£ŗ¼×=ŅŅ£¾±ū | |
| B£® | ČÜŅŗÖŠŅõ”¢ŃōĄė×ÓŗĶĖį·Ö×Ó×ÜŹż£ŗ¼×£¼±ū£¼ŅŅ | |
| C£® | ČÜŅŗpH£ŗ¼×£¼±ū£¼ŅŅ | |
| D£® | ČÜŅŗÖŠŅõ”¢ŃōĄė×Ó×ÜŹż£ŗ¼×£¾±ū£¾ŅŅ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
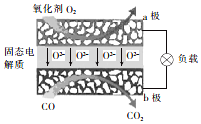 ĪŖĢåĻÖ½ŚÄܼõÅÅµÄĄķÄī£¬ÖŠ¹śŃŠÖĘ³öĮĖŠĀŠĶ¹ĢĢ¬Ńõ»ÆĪļČ¼ĮĻµē³Ų£ØSOFC£©£¬øƵē³ŲµÄ¶”×÷ŌĄķČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ĪŖĢåĻÖ½ŚÄܼõÅÅµÄĄķÄī£¬ÖŠ¹śŃŠÖĘ³öĮĖŠĀŠĶ¹ĢĢ¬Ńõ»ÆĪļČ¼ĮĻµē³Ų£ØSOFC£©£¬øƵē³ŲµÄ¶”×÷ŌĄķČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | µē×Ó“Ób¼«¾µ¼ĻßĮ÷Ļņa¼« | |
| B£® | Õż¼«µÄµē¼«·“Ó¦Ź½ĪŖO2+4e-+2H2OØT4OH- | |
| C£® | »¹æÉŅŌŃ”ÓĆNaOH¹ĢĢå×÷¹ĢĢ¬µē½āÖŹ | |
| D£® | Čō·“Ó¦ÖŠ×ŖŅĘ1 molµē×Ó£¬ŌņÉś³É22.4L£Ø±ź×¼×“æö£©CO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 £¬-C15H27ĪŖĮ“Ģž»ł£¬ŌņĘį·Ó²»Ó¦¾ßÓŠµÄ»ÆѧŠŌÖŹŹĒ£Ø””””£©
£¬-C15H27ĪŖĮ“Ģž»ł£¬ŌņĘį·Ó²»Ó¦¾ßÓŠµÄ»ÆѧŠŌÖŹŹĒ£Ø””””£©| A£® | æÉŅŌøśFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦ | B£® | æÉŅŌŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ« | ||
| C£® | æÉŅŌøśNa2CO3ČÜŅŗ·“Ó¦·Å³öCO2 | D£® | æÉŅŌ·¢ÉśČ”“ś·“Ó¦ŗĶ¼Ó³É·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
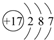 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ö÷×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | O |
| 2 | ¢Ł | ¢Ś | ¢Ū | |||||
| 3 | ¢Ü | ¢Ż | ¢Ž | ¢ß | ¢ą | ¢į |
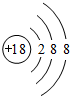 £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šŹōŠŌ±Č¼ŲĒæ | B£® | ×īøß¼ŪŃõ»ÆĪļµÄ»ÆѧŹ½ŹĒSeO3 | ||
| C£® | øß¼Ūŗ¬ŃõĖįµÄĖįŠŌ£ŗH2SeO4£¾H2SO4 | D£® | Ēā»ÆĪļĪČ¶ØŠŌ£ŗH2Se£¾H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
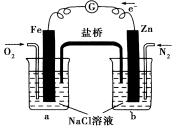
| A£® | ÉÕ±bÖŠ·¢Éś»¹Ō·“Ó¦ | |
| B£® | ÉÕ±bÖŠ·¢ÉśµÄ·“Ó¦ĪŖ2Cl--2e-ØTCl2”ü | |
| C£® | ÉÕ±aÖŠ·¢ÉśµÄ·“Ó¦ĪŖ2H++2e-ØTH2”ü | |
| D£® | ÉÕ±aÖŠµÄČÜŅŗpHÉżøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
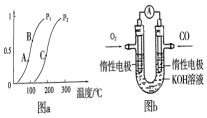 æŖ·¢”¢Ź¹ÓĆĒå½ąÄÜŌ“·¢Õ¹”°µĶĢ¼¾¼Ć”±£¬Õż³ÉĪŖæĘѧ¼ŅŃŠ¾æµÄÖ÷ŅŖæĪĢā£®ĒāĘų”¢¼×“¼ŹĒÓÅÖŹµÄĒå½ąČ¼ĮĻ£¬æÉÖĘ×÷Č¼ĮĻµē³Ų£®
æŖ·¢”¢Ź¹ÓĆĒå½ąÄÜŌ“·¢Õ¹”°µĶĢ¼¾¼Ć”±£¬Õż³ÉĪŖæĘѧ¼ŅŃŠ¾æµÄÖ÷ŅŖæĪĢā£®ĒāĘų”¢¼×“¼ŹĒÓÅÖŹµÄĒå½ąČ¼ĮĻ£¬æÉÖĘ×÷Č¼ĮĻµē³Ų£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com