
【题目】下图所涉及的物质均为中学化学中的常见物质,其中D为黄绿色气体,E为Fe,除D、E、C外余化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
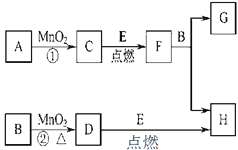
(1)指出MnO2在相关反应中的作用:反应①中是________剂,反应②中是_______剂。
(2)若反应①是在加热条件下进行,则A的化学式是__________;若反应①是在常温条件下进行,则A的化学式是__________。
(3)写出B与MnO2共热获得D的化学方程式_________________________________,该反应中B体现了___________性。
(4)写出F与B反应的离子方程式 ________________________________。
【答案】 催化剂 氧化剂 KClO3 H2O2 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 还原性和酸性 Fe3O4+8H+=Fe2++2Fe3++4H2O
MnCl2+Cl2↑+2H2O 还原性和酸性 Fe3O4+8H+=Fe2++2Fe3++4H2O
【解析】D为黄绿色气体,D是氯气,则B是氯化氢。E为Fe,因此H是氯化铁。铁能在C中燃烧,除D、E、C外其余皆是化合物,所以C是氧气,因此A是双氧水或氯酸钾,F是四氧化三铁,四氧化三铁与盐酸反应生成氯化铁、氯化亚铁和水,所以G是氯化亚铁。
(1)反应①中二氧化锰起催化剂的作用,反应②中浓盐酸被氧化,二氧化锰起氧化剂的作用。(2)若反应①是在加热条件下进行,则A是氯酸钾,化学式是KClO3;若反应①是在常温条件下进行,则A的化学式是H2O2。(3)浓盐酸与MnO2共热获得氯气的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,该反应中氯元素化合价降低,有氯化锰生成,因此浓盐酸体现了还原性和酸性。(4)四氧化三铁与盐酸反应的离子方程式为Fe3O4+8H+=Fe2++2Fe3++4H2O。
MnCl2+Cl2↑+2H2O,该反应中氯元素化合价降低,有氯化锰生成,因此浓盐酸体现了还原性和酸性。(4)四氧化三铁与盐酸反应的离子方程式为Fe3O4+8H+=Fe2++2Fe3++4H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)常温下某溶液中由水电离出的离子浓度符合c(H+)c(OH﹣)=1×10﹣20的溶液,其pH为 , 此时水的电离受到
(2)在某温度下,H2O的离子积常数为1×10﹣13 mol2L﹣2 , 则该温度下:100mL 0.1molL﹣1H2SO4溶液与100mL 0.4molL﹣1的KOH溶液混合后,pH= .
(3)已知一溶液有4种离子:X+、Y﹣、H+、OH﹣ , 下列分析结果肯定错误的是
A.c(Y﹣)>c(X+)>c(H+)>c(OH﹣)
B.c(X+)>c(Y﹣)>c(OH﹣)>c(H+)
C.c(H+)>c(Y﹣)>c(X+)>c(OH﹣)
D.c(OH﹣)>c(X+)>c(H+)>c(Y﹣)
(4)在25℃下,将a molL﹣1的氨水与0.01molL﹣1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl﹣).则溶液显(填“酸”“碱”或“中”)性;用含a的代数式表示NH3H2O的电离常数Kb= .
(5)水溶液中的行为是中学化学的重要内容.已知下列物质的电离常数值:
HClO:Ka=3×10﹣8 H2CO3:Ka1=4.3×10﹣7 Ka2=5.6×10﹣11;84消毒液中通入少量的CO2 , 该反应的化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质一定属于同系物的是( )
① ![]() ②
② ![]() ③
③ ![]() ④C2H4 ⑤CH2=CH﹣CH=CH2 ⑥C3H6 ⑦
④C2H4 ⑤CH2=CH﹣CH=CH2 ⑥C3H6 ⑦ ![]() ⑧
⑧ ![]()
A.①和②
B.④和⑥
C.①和③
D.④和⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种气态烷烃和一种气态烯烃的混合物共10g,平均相对分子质量为25.使混合气通过足量溴水,溴水增重8.4g.则混合气中的烷烃的结构简式是 , 物质的量是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂是重要的工业原料.关于“油脂”的叙述错误的是
A.不能用植物油萃取溴水中的溴
B.皂化是高分子生成小分子的过程
C.和H2加成后能提高其熔点及稳定性
D.水解可得到丙三醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于消去反应的是( )
A.CH2=CH2+HCl ![]() ?CH3CH2Cl
?CH3CH2Cl
B.CH4+Cl2 ![]() CH3Cl+HCl
CH3Cl+HCl
C.nCH2=CH2 ![]()
![]()
D.CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O
CH2=CH2↑+NaBr+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com