
下列叙述正确的是
A.氧化还原反应的本质是元素化合价发生了改变
B.含化合价升高元素的反应物被氧化
C.得到电子的物质被氧化
D.氧化还原反应中,氧化剂和还原剂一定是两种物质
科目:高中化学 来源: 题型:
现有物质的量浓度为18.4 mol/L的浓硫酸20.0 mL,加入铜屑共热一段时间后,冷却,滤去多余的铜屑,将滤液加水到100.0 mL,测得溶液中SO42-的物质的量浓度为3.18 mol/L。试求该100 mL溶液中硫酸铜的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知0.1mol/L的醋酸溶液存在电离平衡:CH3COOH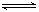 CH3COO- + H+,下列叙述正确的是
CH3COO- + H+,下列叙述正确的是
A.c(H+)+c(CH3COO-)+c(CH3COOH)=0.1mol/L
B.加入少量0.1mol/L的盐酸,电离平衡向左移动,c(H+)减小
C.加入少量NaOH固体,电离平衡向右移动,溶液导电性增强
D.加入少量CH3COONa固体,电离平衡向左移动,溶液导电性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,xA + yB zC,达到平衡,试填写下列空白:
zC,达到平衡,试填写下列空白:
⑴若A、B、C都是气体,减压后向逆反应方向移动,则x、y、z之间的关系是 。
⑵已知C是气体,且x+y=z,加压时平衡如果发生移动,则平衡必向 方向移动。
⑶若B、C是气体,其他条件不变时增加A的用量,平衡不移动,则A的状态为 。
⑷加热后C的百分含量减少,则正反应是 反应(选填“吸热”、“放热”)
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ 在某压强恒定的密闭容器中加入2 molN2和4 molH2,发生如下反应:
N2(g)+3H2(g) 2NH3(g);ΔH=—92.4 kJ/mol。达到平衡时,体积为反应前的三分之二。求:
2NH3(g);ΔH=—92.4 kJ/mol。达到平衡时,体积为反应前的三分之二。求:
(1)达到平衡时,N2的转化率为_______________。
(2)若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c均>0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同。试比较反应放出的能量:
(1)________(2)(填“>”、“<”或“=”)。
Ⅱ 若将2 molN2和4 molH2放入起始体积相同的恒容容器中,在与Ⅰ相同的温度下达到平衡。
试比较平衡时NH3的浓度:Ⅰ________Ⅱ (填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质按化合物、单质、混合物顺序排列的是( )
A、 烧碱、液态氧、碘酒 B、生石灰、熟石灰、白磷
C、 干冰、铜、氯化氢 D、 空气、氮气、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
在四个脱落标签的试剂瓶中,分别盛有盐酸、BaCl2溶液、Na2CO3溶液、AgNO3溶液,为了鉴别各瓶中的试剂,将它们分别编号为A、B、C、D并两两混合,其实验现象为:A+B产生无色气体;B+C产生白色沉淀;A+D产生白色沉淀;A+C无明显变化。
(1)由此推出各试剂瓶所盛放的试剂为(填化学式):
A__________,B__________,C__________,D__________,
(2)A+B反应的离子方程式为______________________________。
(3)A+D反应的离子方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知298K时,2SO2(g)+O2(g)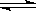 2SO3(g) ΔH=—197kJ/mol,在相同温度下,向固定体积的密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q1;向另一个同体积的密闭容器中通入1molSO2和0.5molO2,达到平衡时放出热量为Q2,则下列关系中正确的是
2SO3(g) ΔH=—197kJ/mol,在相同温度下,向固定体积的密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q1;向另一个同体积的密闭容器中通入1molSO2和0.5molO2,达到平衡时放出热量为Q2,则下列关系中正确的是
A.Q2>Q1/2 B.Q2=Q1/2 C.Q2<Q1<197kJ D.Q2=Q1=197kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com