考点:化学平衡的计算,用盖斯定律进行有关反应热的计算,化学电源新型电池,使用化石燃料的利弊及新能源的开发
专题:化学反应中的能量变化,化学平衡专题,电化学专题
分析:(1)低碳经济以低能耗、低排放、低污染为基础,其实质是提高能源利用效率和创建清洁能源结构,据此回答;
(2)依据盖斯定律解答,从所求反应出发,分析反应物生成物的位置,通过加减可得;
(3)①由表中数据可知,CO的物质的量变化量为4mol-2.4mol=1.6mol,根据v=
计算v(CO),再利用速率之比等于化学计量数之比计算v(CO
2);
②第二组温度比第一组高,反应物物质的量比第一组减半,但是平衡时CO
2的物质的量比第一组的一半少,表明该反应为放热反应;
③反应前后气体体积不变,实验2相似的平衡状态(即各物质的质量分数分别相等),为等效平衡,满足CO(g)与H
2O(g)的物质的量为1:2,由于到达平衡时间t<3min,物质的量应比实验2大或使用催化剂;
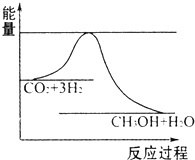
(4)根据图象知,该反应的正反应是放热反应,能使c(CH
3OH)增大,说明平衡向正反应方向移动;
(5)用氢氧化钾溶液作电解质溶液,甲醇在负极上失去电子生成碳酸根离子和水,氧气在正极上得到电子生成氢氧根离子,阳离子移向正极.
解答:
解:(1)a.采用节能技术,减少化石燃料的用量,可减少二氧化碳的排放,符合“低碳”经济理念,故正确;
b.鼓励乘坐公交车出行,倡导节能生活,可减少二氧化碳的排放,符合“低碳”经济理念,故正确;
c.太阳能、风能等新型能源不能替代化石燃料,故错误;
d.新建一批小型火电厂,不会减少二氧化碳的排放,不符合“低碳”经济理念,故错误;
故选ab;
(2)已知
①C(s)+
O
2(g)═CO(g)△H=-126.4kJ?mol
-1②2H
2(g)+O
2(g)═2H
2O(l)△H=-571.6kJ?mol
-1③H
2O(g)═H
2O(l)△H=-44kJ?mol
-1据盖斯定律,①-②×
+③得:C(s)+H
2O(g)═CO(g)+H
2(g)△H=(-126.4kJ?mol
-1)-(-571.6kJ?mol
-1)×
+(-44kJ?mol
-1)=+115.4KJ/mol
故答案为:+115.4KJ/mol;
(3)①由表中数据可知,CO的物质的量变化量为4mol-2.4mol=1.6mol,v(CO)=
≈0.13mol/(L?min),速率之比等于化学计量数之比,故v(CO
2)=v(CO)=0.16mol/(L?min)=0.13mol/(L?min),
故答案为:0.13mol/(L?min);
②实验1中CO的转化率为
×100%=40%,实验2中CO的转化率为
×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,正反应放热,逆反应是吸热反应;实验2条件下,CO的物质的量变化量为4mol-2.4mol=1.6mol,所以CO
2、H
2的物质的量变化量为1.6mol,平衡常数K=
≈0.17,
故答案为:吸;0.17;
③反应前后气体体积不变,实验2相似的平衡状态(即各物质的质量分数分别相等),为等效平衡,满足CO(g)与H
2O(g)的物质的量为1:2,即a:b=1:2,b=2a,由于到达平衡时间t<3min,所以速率较实验2快,故a>0.5(或使用催化剂).
故答案为:b=2a,a>0.5(或使用催化剂).
(4)a.升高温度,平衡逆向移动,c(CH
3OH)减小,故a错误;
b.充入He(g),使体系压强增大,由于容器为恒容容器,各组分浓度不变,平衡不移动,c(CH
3OH)不变,故b错误;
c.将H
2O(g)从体系中分离出来,平衡正向移动,c(CH
3OH)增大,故c正确;
d.再充入1mol CO
2和3molH
2,平衡正向移动,c(CH
3OH)增大,故d正确.
故答案为:cd;
(5)用氢氧化钾溶液作电解质溶液,甲醇在负极上失去电子生成碳酸根离子和水,负极反应为CH
3OH-6e
-+8 OH
-═CO
32-+6H
2O,氧气在正极上得到电子生成氢氧根离子,通入氧气的电极应为正极,阳离子钾离子移向正极,故答案为:正;正.
点评:本题考查反应速率、平衡常数、化学平衡以及热化学和电化学的有关计算应用,难度中等,注意对知识的理解与掌握,是对学生能力的考查.

 国务院总理温家宝在哥本哈根世界气候峰会上表示,中国正处于工业化、城镇化快速发展的关键阶段,能源结构以煤为主,降低排放存在特殊困难,但仍始终把应对气候变化作为重要战略任务.现在“低碳循环”已经引起了国民的重视,试回答下列问题:
国务院总理温家宝在哥本哈根世界气候峰会上表示,中国正处于工业化、城镇化快速发展的关键阶段,能源结构以煤为主,降低排放存在特殊困难,但仍始终把应对气候变化作为重要战略任务.现在“低碳循环”已经引起了国民的重视,试回答下列问题:

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案


 属于加成反应
属于加成反应