
【题目】下列应用与水解原理无关的是
A. 实验室盛放碳酸钠溶液的试剂瓶不能用玻璃塞
B. 泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将两者混合就可产生大量二氧化碳的泡沫
C. 浓硫化钠溶液有臭味
D. 可用碳酸钠与醋酸制取少量二氧化碳
【答案】D
【解析】
A. 在碳酸钠溶液中,碳酸根离子会发生水解,使溶液呈碱性,则不能用玻璃塞的试剂瓶盛放碳酸钠溶液;
B. 泡沫灭火器利用的是碳酸氢钠与硫酸铝发生双水解反应;
C. 浓硫化钠溶液中,硫离子发生两步水解生成硫化氢气体;
D. 醋酸的酸性大于碳酸,则用醋酸与碳酸钠反应制取二氧化碳。
A. 碳酸钠水解呈碱性,可与二氧化硅反应生成硅酸钠而导致玻璃塞打不开,实验室盛放碳酸钠溶液的试剂瓶不能用玻璃塞,与水解原理有关,不符合题意,故A项不选;
B. 碳酸氢钠溶液和硫酸铝发生互促水解反应而生成二氧化碳气体,可用于灭火,与盐的水解原理有关,不符合题意,故B项不选;
C. 硫离子发生两步水解,其水解离子方程式为:S2-+ H2O![]() HS-+ OH-,HS-+ H2O
HS-+ OH-,HS-+ H2O![]() H2S+ OH-,浓硫化钠溶液中生成硫化氢气体,与盐的水解原理有关,不符合题意,故C项不选;
H2S+ OH-,浓硫化钠溶液中生成硫化氢气体,与盐的水解原理有关,不符合题意,故C项不选;
D. 醋酸酸性比碳酸弱,可用碳酸钠与醋酸制取少量二氧化碳,该反应利用了强酸制弱酸的原理,与盐类水解无关,符合题意,故D项选;
答案选D。


科目:高中化学 来源: 题型:
【题目】把1 mol X气体和0.5 mol Y气体混合于2 L密闭容器中,发生如下反应:3X(g)+Y(g)![]() nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
(1)前2 min内,用X表示的平均反应速率________;
(2)2 min末时Y的转化率________;
(3)化学方程式中Z的化学计量数n________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酯类化合物G是一种香料,以丙酮为初始原料合成该有机物的流程如下图所示(部分产物及反应条件已略去):
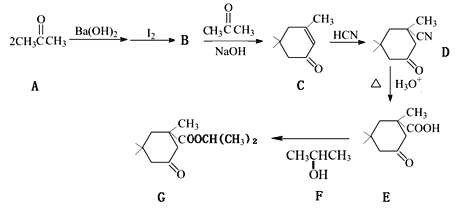
已知:![]()
(1)B的结构简式为______________,F的名称是__________。
(2)C中含氧官能团的名称是______________。
(3)C转化成D的反应类型_________________。
(4)D的分子式为_______________________。
(5)E转化成G的化学方程为________________。
(6)芳香化合物H比C少两个氢原子,能与氯化铁溶液反应显紫色且苯环上的一氯代物只有一种,写出满足上述条件的H的所有同分异构体的结构简式__________。H的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是____(填序号)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
(7)设计以CH3CH2CH2OH为起始原料制备2-甲基丙酸(![]() )的合成路线__(无机试剂任选)。
)的合成路线__(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C三种无色溶液,它们分别是葡萄糖溶液、蔗糖溶液、淀粉溶液中的一种,某同学做实验得出:
①B能发生银镜反应;②A遇碘水变蓝色;③A、C均能发生水解反应,水解液均能发生银镜反应。
回答下列问题:
(1)写出各物质的名称:
A是________,B是________,C是________。
(2)写出有关化学反应方程式:
①蔗糖水解:__________________________________________。
②淀粉水解:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,将4.48L的NO2和NO组成的混合气体通入100mL的水中,气体体积缩小为2.24L,假设溶液的体积不变,则下列说法中错误的是( )
A.所得溶液中溶质的物质的量浓度为1.0mol·L-1
B.剩余气体中氮元素与氧元素的质量为7∶8
C.原混合气体中NO2和NO的体积比为1∶1
D.反应过程中转移的电子总数为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为了证明、比较SO2和氯水的漂白性,设计了如图所示的实验装置。

(1)实验室常选用KMnO4和浓盐酸制Cl2;选用Cu和浓硫酸反应制取SO2时,其中制SO2应选用如图A、E两发生装置中___装置(填装置序号),反应的化学方程式为___。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:___,D:___。
(3)甲乙两名同学分别利用如图所示装置探究两种气体按不同比例混合后的漂白性。

试
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是:___。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是:___(结合反应方程式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置,完成很多电化学实验。下列有关此装置的叙述中,正确的是

A. 若X为碳棒,Y为NaCl溶液,开关K置于N处,可加快铁的腐蚀
B. 若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极保护法
C. 若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D. 若X为铜棒,Y为硫酸铜溶液,开关K置于N处,可用于铁表面镀铜,溶液中铜离子浓度将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2升的密闭容器中,发生以下反应:2A(g)+ B(g)![]() 2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.16 mol/(L·s),则10秒钟时,容器中B的物质的量是
2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.16 mol/(L·s),则10秒钟时,容器中B的物质的量是
A. 1.6 mol B. 2.8 mol C. 2.4 mol D. 1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与金属腐蚀有关的说法正确的是( )

A. 图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B. 图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小
C. 图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D. 图d中,钢铁轮船外壳连接一块金属A(铜块)可以减缓船体外壳腐蚀速度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com