
【题目】下列关于胶体的说法正确的是( )
A. 依据丁达尔效应可将分散系分为溶液、胶体与浊液
B. 向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O![]() Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
C. Na+、K+、SO42-、Br-能在Fe(OH)3胶体中大量共存
D. 沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将反应Cu(s)+2Ag+(aq)===Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,下列有关叙述正确的是( )

A、KNO3盐桥中的K+移向Cu(NO3)2溶液
B、Cu作负极,发生还原反应
C、电子由AgNO3溶液通过盐桥移向Cu(NO3)2溶液
D、工作一段时间后,AgNO3溶液中c(Ag+)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国规定:室内甲醛含量不得超过0.08mg·m-3。某研究性学习小组欲利酸性KMnO4溶液测定空气中甲醛的含量, (部分装置如图),其反应原理及步骤如下:
4MnO4-+5HCHO+H +=Mn2++5CO2↑+11H2O
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O

步骤:①量取5.00mL 1.00×10-3mol·L-1 KMnO4,溶液于洗气瓶中,并滴入几滴稀H2SO4,加水20mL稀释备用。
②取1.00×10-3mol·L-1草酸标准溶液于酸式滴定管中备用。
③用注射器抽取100mL新装修室内空气。再将注射器气体推入洗气瓶中充分反应。再重复4次。
④将洗气瓶中溶液转移到锥形瓶中(包括洗涤液),再用标准草酸溶液进行滴定,记录滴定所消耗的草酸溶液的体积。
⑤再重复实验2次(每次取高锰酸钾溶液5.00mL)。3次实验消耗草酸溶液的体积平均值为12.38mL。
回答下列问题
(1)此实验用指示剂____________(填字母)。A 甲基橙 b酚酞 c淀粉 d无需另外添加试剂
(2)量取5.00mL KMnO4溶液应用______________滴定管
(3)下列操作能引起室内甲醛浓度偏高的是________。
a.滴定终点俯视读数 b.滴定前有气泡滴定后无气泡
c.在高锰酸钾溶液中加入少量水 d.装草酸的滴定管未润洗
(4)草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,如果向10 mL 0.01 molL-1 H2C2O4溶液中滴加0.0 1 molL-1 NaOH溶液
①当加入的NaOH溶液体积为10 mL,请你写出溶液中质子守恒关系式__________。
②当加入的NaOH溶液体积为20 mL,请你写出溶液中离子的浓度大小关系__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是材料、能源、环境、信息等现代科学技术的重要基础。下列说法不正确的是
A. 制造矢量发动机使用含铼(Re)合金材料,合金是纯净物
B. “人造太阳”的核燃料是氘、氚,12H、13H互为同位素
C. 在人体中检测出了“微塑料”,说明白色污染危害严重
D. 制造芯片的工艺中,用氢氟酸腐蚀硅是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是________;
(2)X与金属钠反应放出氢气,反应的化学方程式是____________(有机物用结构简式表达);
(3)X与空气中的氧气在铜或银催化作用下反应生成Y,Y的结构简式是________;
(4)X与高锰酸钾酸性溶液反应可生成Z,Z的名称为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中将1 mol CH4和适量O2混合点燃,充分反应后,CH4和O2均无剩余,且产物均为气体,质量为72 g,下列叙述正确的是 ( )
A. 若将产物通过碱石灰,则可全部被吸收;若通入浓硫酸,则不能完全被吸收
B. 产物的平均摩尔质量为20g·mol-1
C. 若将产物通过浓硫酸后恢复至室温,压强变为反应前的1/3
D. 反应中消耗O2 56g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[物质结构与性质一选修3]
种类繁多的碳族元素的单质及其化合物,有着重要的研究价值。
(1)锗(Ge)的含量十分稀少,但它被广泛应用于电子、光学、化工、生物医学、能源及其他高新科技领域。
①现代化学中,常利用__________上的特征谱线来鉴定元素。基态锗原子中,核外能级最高的原子轨道上,具有的电子数为___________。
②通常状况下GeCl4是无色液体,易挥发,其熔点为-51.50C,沸点为86.55℃,能溶于乙醚。由此可推知GeCl4应属于共价化合物,其理由是_______,也即氯和锗两元素的电负性相差应该_______1.7(填“小于”或“大于”)。
(2)在硅酸盐中,![]() 如图a所示为四面体结构,它可以通过公用顶角0原子,形成链状层状、岛状和网状结构的不同硅酸盐。图b表示由n个四面体连接成的硅酸根,其中Si的杂化形式为_____,Si与O的原子个数比为________,化学式可表示为__________。
如图a所示为四面体结构,它可以通过公用顶角0原子,形成链状层状、岛状和网状结构的不同硅酸盐。图b表示由n个四面体连接成的硅酸根,其中Si的杂化形式为_____,Si与O的原子个数比为________,化学式可表示为__________。

(3)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图(a)所示。图(b)是一个石墨的六方晶胞示意图。

①请在图 中画出晶胞沿c轴的投影 (用“·”标出碳原子位置即可)_________。
中画出晶胞沿c轴的投影 (用“·”标出碳原子位置即可)_________。
②假设石墨晶胞高为h cm,C-C键长为r cm,则石墨晶体密度的表达式为__________g.cm-3(阿伏加德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10℃时某化学反应速率为0.1mol/ (L·s),若温度每升高10℃反应速率增加到原来的2倍。为了把该反应速率提高到1.6 mol/(L·s),则该反应需在什么温度下进行
A. 30℃ B. 40℃ C. 50℃ D. 60℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学设计如下实验方案,以分离KCl和BaCl2的固体混合物,试回答下列问题:
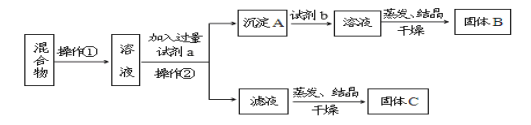
供选择的试剂有:盐酸、硫酸钾溶液、碳酸钾溶液、碳酸钠溶液
(1)操作①的名称是_____,操作②的名称是_____。
(2)试剂a是_____,试剂b是_____,固体B化学式_____。
(3)加入试剂a所发生的化学反应方程式为:____。加入试剂b所发生的化学反应方程式为:___。
(4)乙同学认为该方案不能达到实验目的,理由是:_____ ;应如何改进____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com