
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如右图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是

A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性: Z>W>X
C. 4种元素的单质中,Z单质的熔、沸点最高
D. W单质能与水反应,生成一种具有漂白性的物质
【答案】CD
【解析】X、Y、Z、W均为短周期元素,Y原子的最外层电子数是次外层电子数的3倍,由于最外层电子数不能超过8,Y原子只能有2个电子层,次外层电子数为2,最外层电子数为6,则Y为O元素;由图中的位置可知,X为N元素,Z为S元素,W为Cl元素。A.同周期元素的从左到右原子半径逐渐减小,则X>Y,Z>W,同主族元素从上到下原子半径逐渐增大,且原子核外电子层数越多,半径越大,则W>X,所以原子半径大小顺序为Z>W>X>Y,故A错误;B.同周期元素从左到右元素的非金属性逐渐增强,元素的非金属性越强,对应最高价氧化物的水化物的酸性越强,可知最高价氧化物对应水化物的酸性:W>Z,故B错误;C.四种元素的单质中,常温下Z的单质是固体,其余均是气体,Z单质硫的熔、沸点最高,故C正确;D.氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,HCl没有漂白性,故D正确;故选CD。


科目:高中化学 来源: 题型:
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是海水综合利用的一个方面。

Ⅰ.(1)上述过程中没有涉及到的四大基本反应类型是 ______;
a.化合反应 b.分解反应 c.置换反应 d.复分解反应
(2)步骤1中分离操作的名称是___________;
(3)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Na2CO3溶液
加入试剂的顺序是_____________;
II.实验室利用精盐配制480mL 2.0mol·L1NaCl溶液。
(4)除容量瓶外,还需要的玻璃仪器有___________________;
(5)用托盘天平称取固体NaCl________g;
(6)配制时,按以下几个步骤进行:①计算 ②称量 ③溶解 ④冷却 ⑤转移 ⑥定容 ⑦摇匀 ⑧装瓶。操作中还缺少一个重要步骤是______________________;
(7)下列错误操作可使所配制氯化钠溶液浓度偏低的是(_________)
a.容量瓶洗净后残留了部分的水
b.转移时溶液溅到容量瓶外面
c.定容时俯视容量瓶的刻度线
d.摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的金属Na、Mg、Al分别与100mL 2molL-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法不正确的是( )
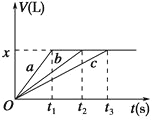
A. x=2.24
B. 三种金属的物质的量均为0.2 mol
C. 反应时,Na、Mg、Al均过量
D. 曲线b为Mg与盐酸反应的图象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A. 23g Na 与足量H2O反应完全后可生成NA个H2分子
B. 1 molCu和足量热浓硫酸反应可生成NA个SO3分子
C. 标准状况下,22.4LN2和H2混合气中含NA个原子
D. 3mol单质Fe完全转变为Fe3O4,失去8NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在20℃时,将4.95gKNO3溶于10.0g水中,恰好配成密度为1.15g/cm3的饱和溶液,计算:
(1)此饱和溶液中KNO3的物质的量为_______;
(2)此饱和溶液中KNO3的物质的量浓度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用如图所示装置探究SO2的性质及其有关实验。

(1)实验室用亚硫酸钠固体和一定浓度的硫酸反应制备SO2 气体,写出该反应的化学方程式________
(2)分别将SO2 气体通入下列C 溶液中,请回答下列问题:
①少量SO2通入紫色石蕊试液,现象是_______,继续通入过量SO2 气体,现象是____________
②SO2 通入紫色KMnO4溶液,现象是_______,其反应的离子方程式为__________
③过量SO2慢慢地通入澄清石灰水中,现象是_________
④若C为双氧水,则通入SO2 后,请大胆判断所得溶液是_______(填溶质的化学式),若该同学制备的SO2 气体中混有CO2 气体,产生杂质的原因可能是亚硫酸钠固体中混有______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组内物质的转化,只通过一步反应不能完成的是( )
A. Zn→H2 B. Cu→Cu(OH)2
C. CO2→CaCO3 D. KMnO4→MnO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于反应2KClO3+I2=2KIO3+Cl2的叙述中正确的是( )
A.该反应属于置换反应B.氧化性:I2>KClO3
C.还原性:KClO3>I2D.还原剂为KIO3,氧化剂为I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置,设计实验,验证浓硫酸与木炭粉反应所生成的气体产物
序号 | ① | ② | ③ | ④ |
装 置 |
|
|
|
|
(1)浓硫酸与木炭粉在加热条件下的化学方程式为_____________________
(2)已知KMnO4 酸性溶液可以吸收SO2,试用上图中各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向) 是(填装置的编号):_____________________________________
(3)实验时可观察到装置①中A 瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用___________,B瓶溶液的作用________________C 瓶溶液的作用是______________
(4)裝置③中所盛溶液是_______,可验证的产物是__________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com