
����ͼ��ʾ��ͼ���Ǻ�ѹ�ܱ�������ͼ���Ǻ����ܱ�������������������ͬʱ���ڢ��зֱ����2 mol X��2 mol Y����ʼʱ�����������ΪV L���������·�Ӧ���ﵽƽ��״̬����ʾ������X��Y��״̬��δ֪������Z��״̬Ϊ��̬����2X������+ Y������![]() a Z��g��
a Z��g��
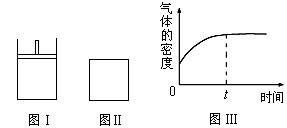
��ʱ����X��Y��Z�����ʵ���֮��Ϊ1��3��2�������ж���ȷ����
A������Z�Ļ�ѧ������a = 2
B��������������ܶ���ͼ����ʾ����X��Y��ֻ��һ��Ϊ��̬
C����X��Y��Ϊ��̬������ƽ��ʱX��ת���ʣ���
D����XΪ��̬��YΪ��̬������дӿ�ʼ��ƽ�������ʱ�䣺��
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ �� | �й���Ϣ |
| A | ����������Ӧ��ˮ����ף���������̬�⻯��ң���Ӧ������ |
| B | �����������Ǵ�����������2�� |
| C | M������3������ |
| D | ������ԭ�Ӱ뾶��������Ԫ�� |
| E | �������������۴�����Ϊ6 |

 A2O4��g������H��0���ں��º��������£���һ����AO2��A2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������У���Ӧ�����и����ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ����ͼ��ʾ��
A2O4��g������H��0���ں��º��������£���һ����AO2��A2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������У���Ӧ�����и����ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�걱����101��ѧ�߶���ѧ�����п��Ի�ѧ�Ծ����������� ���ͣ������
��10�֣����ݵ���������Ӧ���Ȼ�ѧ����ʽ�������ж���ȷ����
�� I2��g����H2��g�� 2HI��g����H����9.48 kJ/mol
2HI��g����H����9.48 kJ/mol
�� I2��s����H2��g�� 2HI��g����H����26.48 kJ/mol
2HI��g����H����26.48 kJ/mol
��1��д����̬��������̬����Ȼ�ѧ����ʽ�� ��
��2������Ӧ������52.96kJ����ʱ��ת�Ƶ��ӵ����ʵ����� mol��
��3�������ں��¡������ܱ������н��еķ�Ӧ�٣���˵����ﵽ��ѧƽ��״̬���� ��
A. ����������ѹǿ����
B. �����������ܶȲ���
C. ������������ɫ����dz����
D. ��n��H��H�����ѵ�ͬʱ��2n��H��I������
��4����ͨ����Ӧ2NO��O2��2NO2��NO2��2H����2I����NO��I2��H2O����ȡ�⣬NO���Ƶ�����е������� ��
��5�����Ṥҵβ���ж�������ĺ�������0.05%�����������ʱ�辭����������ŷš�ijУ��ѧ��ȤС�����ⶨij���Ṥ���ŷ�β���ж�������ĺ������������·���������ͼ��ʾ��ͼ������������B����ȷ����ͨ����β���������β��ͨ��һ�������֪Ũ�ȵĵ�ˮ�вⶨSO2�ĺ�������ϴ��ƿC����Һ����ɫ��ʧʱ�������رջ���A��
���õ�ˮ�ⶨSO2�ĺ����Ļ�ѧ����ʽ�� ��
��ϴ��ƿC�е���ĩ������һ���������D���������ʵ���ȷ�ȣ��������� ��
��ϴ��ƿC����Һ����ɫ��ʧ��û�м�ʱ�رջ���A����õ�SO2����_________���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012��㶫ʡ������������ѧ����10���¿������ۺϻ�ѧ�Ծ����������� ���ͣ�������
��16�֣��״������͵���������ȼ�ϡ���ҵ�Ͽ�ͨ��H2��CO�����Ʊ��״����÷�Ӧ���Ȼ�ѧ����ʽΪ��2H2(g)��CO(g) CH3OH(g)
CH3OH(g) 
��1����֪��



1 mol�״�������ȫȼ������CO ��ˮ�������Ȼ�ѧ����ʽΪ ��
��ˮ�������Ȼ�ѧ����ʽΪ ��
��2�����д�ʩ�����������2H2(g)��CO(g) CH3OH(g)��Ӧ���ʵ��� ��˫ѡ)��
CH3OH(g)��Ӧ���ʵ��� ��˫ѡ)��
| A�������CH3OH | B�������¶� | C����Сѹǿ | D��������ʵĴ��� |

 CH3OH(g)��ƽ�ⳣ������д��������̣�
CH3OH(g)��ƽ�ⳣ������д��������̣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�콭��ʡ�����и߶���ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ������
�ҹ��зḻ����Ȼ����Դ������Ȼ��Ϊԭ�Ϻϳ����ص���Ҫ��������ͼ��ʾ��ͼ��ijЩת�����輰������δ�г�����

��1������ϳ������������Ȼ�ѧ����ʽ��CH4(g)+H2O(g)  CO(g)+3H2(g)����H��0
CO(g)+3H2(g)����H��0
�ں��º��ݵ������£������CH4�ķ�Ӧ���ʺ�ת���ʣ����д�ʩ���е��� ��
A������ѹǿ B�������¶� C������He�� D������ˮ����Ũ��
��2����ת��һ����̼�������ķ���ʽ��H2O(g) +CO(g)  H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
|
�¶�/�� |
400 |
500 |
800 |
|
ƽ�ⳣ��K |
9.94 |
9 |
1 |
�����̼��[ n��H2O��/n��CO��]��Kֵ ������������䡱��С���������÷�Ӧ��400��ʱ���У���ʼͨ������ʵ�����H2O��CO����Ӧ���е�ijһʱ��ʱCO��CO2��Ũ�ȱ�Ϊ1��3����ʱv������ v���棩�����������������������
��3���йغϳɰ���ҵ��˵������ȷ���� ��
A���÷�Ӧ�����˹��̵�
B���ϳɰ���ҵ��ʹ�ô�������߷�Ӧ���������
C���ϳɰ���Ӧ�¶ȿ�����500�����ң�Ŀ����ʹ��ѧƽ��������Ӧ�����ƶ�
D���ϳɰ���ҵ����ѭ����������Ҫԭ����Ϊ�˼ӿ췴Ӧ����
��4���������ع����У�������n(NH3)��n(CO2)��������Ϊ ����ʵ�����������У�����ʹn(NH3)��n(CO2)��3��������Ϊ ��
��5��������ϳɰ�����ת����Ϊ60��ʱ����3.0��108 L����Ϊԭ���ܹ��ϳ� L ������������������ڱ�״���²ⶨ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ģ���� ���ͣ�������ѡ����
 aZ(g) ��ʱI��X��Y��Z�����ʵ���֮��Ϊ1:3:2�������ж���ȷ����
aZ(g) ��ʱI��X��Y��Z�����ʵ���֮��Ϊ1:3:2�������ж���ȷ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com