
| A. | 哈伯法合成氨是吸热反应,新法合成氨是放热反应 | |
| B. | 新法合成和哈伯法相比不需要在高温条件下,可节约大量能源,具有发展前景 | |
| C. | 新法合成能在常温下进行是因为不需要断裂化学键 | |
| D. | 新的催化剂升高了反应所需要的能量,提高了活化分子百分数 |
分析 A.合成氨都是放热反应,催化剂不会改变反应热;
B.根据题目给出信息“在常温下合成氨”来分析解答;
C.化学反应都涉及旧键的断裂和新键的生成;
D.加入催化剂,能降低反应所需要能量,增大活化分子数目,进而增大反应速率.
解答 解:A.哈伯法合成氨和新法合成氨都是放热反应,使用催化剂不会改变反应热,故A错误;
B.题目给出信息“在常温下合成氨”,所以不需要在高温条件下,可节约大量能源,具有发展前景,故B正确;
C.化学反应的本质为原子的重新组合,所以任何化学反应都涉及旧键的断裂和新键的生成,故C错误;
D.催化剂能降低反应的活化能,提高活化分子百分数,不是新的催化剂升高了反应所需要的能量,故D错误.
故选B.
点评 本题主要考查催化剂对化学反应的影响因素以及与反应热间的关系等知识,注意题干信息的应用,主要催化剂能降低反应所需要能量,增大活化分子数目,为高频考点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | C生成的速率与C分解的速率相等 | |
| B. | 单位时间内生成a mol A,同时生成2a mol B | |
| C. | 容器内各组分的总质量不再变化 | |
| D. | 混合气体的总物质的量不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键 分子间作用力 非极性键 | B. | 氢键 氢键 极性键 | ||
| C. | 氢键 极性键 分子间作用力 | D. | 分子间作用力 氢键 非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

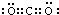 、
、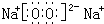 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:实验题
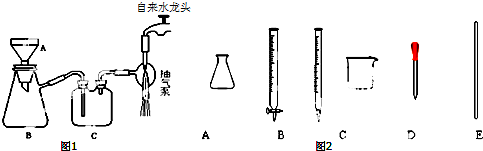
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
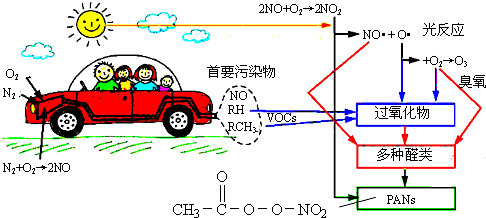
| A. | 汽车尾气中的NO、碳氢化合物(图中RH和RCH3)均来自燃油 | |
| B. | 醛类、PANs(过氧乙酰硝酸酯)均属于无机物 | |
| C. | O3污染、硝酸型酸雨及雾霾均与汽车尾气排放无关 | |
| D. | 汽车启动后,气缸内温度越高,单位时间内NO排放量越大,原因之一是N2与O2的反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
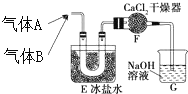 三种常见短周期元素组成的化合物甲,是有机合成中的重要试剂.常温下为黄色气体,具有刺鼻恶臭味,遇水和潮气分解.标况下测定其密度为2.92g/L.浓硝酸与浓盐酸混合制王水过程中会产生少量甲气体、黄绿色气体A和水.
三种常见短周期元素组成的化合物甲,是有机合成中的重要试剂.常温下为黄色气体,具有刺鼻恶臭味,遇水和潮气分解.标况下测定其密度为2.92g/L.浓硝酸与浓盐酸混合制王水过程中会产生少量甲气体、黄绿色气体A和水.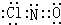 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com