
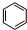
 ����CH3CH2OH
����CH3CH2OH +HO-NO2$��_{��}^{Ũ����}$
+HO-NO2$��_{��}^{Ũ����}$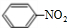 +H2O
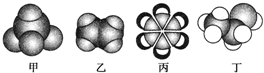
+H2O���� �ɱ���ģ�Ϳ�֪��ΪCH4����ΪCH2=CH2����Ϊ ����ΪCH3CH2OH��
����ΪCH3CH2OH��
��ϩ����̼̼˫���ɷ����ӳɷ�Ӧ��������Ũ������Ũ�����������������������Ҵ������ǻ����ɷ�������������ȩ��
��� �⣺��1���ɱ���ģ�Ϳ�֪��ΪCH4����ΪCH2=CH2����Ϊ ����ΪCH3CH2OH��
����ΪCH3CH2OH��
�ʴ�Ϊ��CH4��CH2=CH2�� ��CH3CH2OH��
��CH3CH2OH��
��2����ϩ����̼̼˫���ɷ����ӳɷ�Ӧ������ʽΪBr2+CH2=CH2��BrCH2-CH2Br��
��Ũ���������£�����Ũ���ᷢ��ȡ����Ӧ��������������Ӧ����ʽΪ�� +HO-NO2$��_{��}^{Ũ����}$
+HO-NO2$��_{��}^{Ũ����}$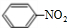 +H2O��
+H2O��
�Ҵ��������������ǻ��ϵ�������ǻ�������̼�ϵ�����ȥ������ȩ����Ӧ�Ļ�ѧ����ʽΪ��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
�ʴ�Ϊ��Br2+CH2=CH2��BrCH2-CH2Br�� +HO-NO2$��_{��}^{Ũ����}$
+HO-NO2$��_{��}^{Ũ����}$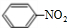 +H2O��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
+H2O��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
���� ���⿼���л���Ľṹ�����ʣ�Ϊ��Ƶ���㣬ע����ݽṹģ���ƶ��л��ע�����չ����ŵ�������ת���ǹؼ���ּ�ڿ���ѧ���Ի���֪ʶ�����գ�


 ��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8�� | B�� | 10�� | C�� | 11�� | D�� | 13�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������



 +2H2O��
+2H2O��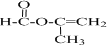 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ǣ�C6H12O6�������ǣ�C12H22O11�� | B�� | ��������������C2H4O2�� | ||
| C�� | �Ҵ����ȩ��CH2O�� | D�� | �����ѣ�C2H6O�������ᣨC3H6O3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȼ�� | B�� | ԭ�ӽ�ϳɷ��� | ||
| C�� | �ֽⷴӦ | D�� | ���ȵ�̼�������̼��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H1-��H2 | B�� | ��H2-��H1 | C�� | ��H1+��H2 | D�� | -����H1-��H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
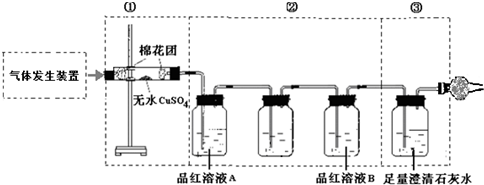
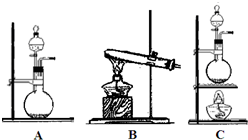
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
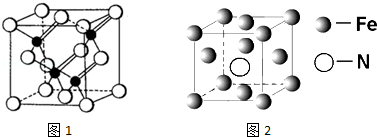
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
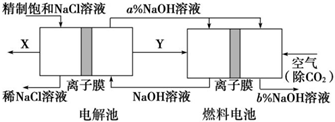
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com