
| ��ѧʽ | ���볣����25�棩 |
| HCN | K=4.9��l0-10 |
| CH3COOH | K=1.8��l0-5 |
| H2CO3 | K1=4.3��l0-7��K2=5.6��l0-11 |
���� ��1��25��ʱ����0.1L 0.2mol•L-1��HA��Һ�У���0.001mol��HA��������ӣ�������Ũ��Ϊ0.01mol/L������pH=-lgc��H+�����㣻
��2����Һ�����ԣ���c��H+��=c��OH-�������ݵ���غ��ж�����Ũ�ȣ�
��3������ˮ�м���pH=1�����ᣬ�Ұ�ˮ������������Ϊ1��1�������ǡ�÷�Ӧ��������泥��������ǿ�������Σ�����Һ�����ԣ���ϵ���غ��ж�����Ũ�ȴ�С˳��
��4����ĵ��볣�����з����жϣ����볣��Խ��Ӧ�ε�ˮ��̶�ԽС����Һ��pHԽС����NaCN��Һ��ͨ������CO2���������ԣ�H2CO3��HCN��HCO3-���ʷ�Ӧ����HCN��̼�����ƣ�
��5�������������������Ʒ�Ӧ������ǡ�ó�������ҪBa��OH��2��NaHSO4�������ʵ���1��1��Ӧ�������Һ��pH����Һ����������ʵ�����ʽ���㣻
��� �⣺��1����0.1L 0.2mol•L-1��HA��Һ�У���0.001mol��HA��������ӣ���c��H+��=$\frac{0.001mol}{0.1L}$=0.01mol/L������pH=2��
�ʴ�Ϊ��2��
��2�������Һ�����ԣ�����c��H+��=c��OH-�������ݵ���غ��c��NH4+��+c��H+��=2c��SO42-��+c��OH-��������c��SO42-��=$\frac{1}{2}$c��NH4+��=0.5amol•L-1��
�ʴ�Ϊ��0.5amol/L��
��3������ˮ�м���pH=1�����ᣬ�Ұ�ˮ������������Ϊ1��1�������ǡ�÷�Ӧ��������泥������Ϊǿ�������Σ�笠�����ˮ���ʹ����Һ�����ԣ�pH��7��ˮ�����ӷ���ʽΪNH4++H2O?NH3•H2O+H+����Һ��������c��H+����c��OH-������Һ�д��ڵ���غ�c��H+��+c��NH4+��=2c��SO42-��+c��OH-�������� c��NH4+����c��SO42-����笠�����ˮ��̶Ƚ�С������c��SO42-����c��H+����������Ũ�ȴ�С˳���� c��NH4+����c��SO42-����c��H+����c��OH-����
�ʴ�Ϊ��c��NH4+����c��SO42- ����c��H+����c��OH-����
��4������ͼ�����ݷ��������볣�������HCN��̼��������ӣ����Ե�Ũ�ȵ�NaCN��Һ��Na2CO3��Һ��CH3COONa��Һˮ��̶�Ϊ��Na2CO3��Һ��NaCN��Һ��CH3COONa��Һ������Һ��pHΪ��Na2CO3��Һ��NaCN��Һ��CH3COONa��Һ����NaCN��Һ��ͨ������CO2���������ԣ�H2CO3��HCN��HCO3-���ʷ�Ӧ����HCN��̼�����ƣ��������ɶ�����̼���ʷ�Ӧ�Ļ�ѧ����ʽΪNaCN+H2O+CO2=HCN+NaHCO3��
�ʴ�Ϊ��Na2CO3��Һ��NaCN��Һ��CH3COONa��Һ��?NaCN+H2O+CO2=HCN+NaHCO3��
��5��pH=12��Ba��OH��2��Һ��C��OH-��=10-2mol/L������Һ���Ϊx���õ��������������ʵ���Ϊx��10-2mol����Ӧ�������������ʵ���Ϊ0.5x��10-2mol��������������Һ���Ϊy�����ݷ�ӦBa��OH��2+NaHSO4=BaSO4��+H2O+NaOH����Ϻ���ҺpH=11������õ���Һ������������Ũ��Ϊ10-3mol/L��
���Եõ���$\frac{x��1{0}^{-2}-0.5x��1{0}^{-2}}{x+y}$=10-3��
�õ�x��y=1��4��
�ʴ�Ϊ��1��4��
���� ���⿼������Ӧ���ۺϼ��㣬��ҺpH�ļ���Ӧ�ã�ע����Һ������������Ũ�Ⱥ�����Ũ�ȵĹ�ϵ�ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 ��Ȥ������ҵ���ϿƼ�������ϵ�д�
��Ȥ������ҵ���ϿƼ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���еķ�Ӧ�� | ���е����� | ʵ����� | 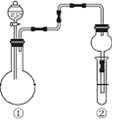 | |
| A | ���ϡ���� | ��������Һ�г��ְ�ɫ���� | ���ԣ����̼����� | |
| B | MnO2��Ũ���� | ����KI��Һ���� | Cl2�������� | |
| C | Na2SO3������ | ��ˮ��ɫ | SO2��Ư���� | |
| D | Cu������ | ����ɫ���� | ��������ΪŨ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��Һ��c��H+����c��OH-�� | |
| B�� | NH4+ˮ�������� | |
| C�� | NH3•H2O������ | |
| D�� | ��H2O�������c��H+����10-7 mol/L | |
| E�� | ���ʵ���Ũ����ȵİ�ˮ������������ϣ���ҺpH=7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH��Һ | B�� | ��ˮ | C�� | ����ʯ��ˮ | D�� | Mg��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 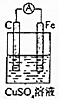 ʵ�飺������Aָ��ƫת��̼�����к�ɫ�������� | |
| B�� | 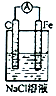 ʵ�飺������Aָ��ƫת������������ɫ������� | |
| C�� | 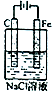 ʵ�飺̼��������ɫ����������������л���ɫ������� | |
| D�� | 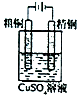 ʵ�飺��ͭ���к�ɫ������������ͭ�ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H1����H3 | B�� | ��H3=��Hl+��H2 | ||
| C�� | ��Ӧ�ٵĻ��Ϊ24.4 kJ•mol-1 | D�� | ��Ӧ��һ�������Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ����0.1mol/L��NaNO3��Һ | B�� |  ���װ�������� | ||
| C�� | 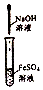 ��ȡFe��OH��2���� | D�� | 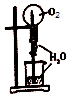 ������Ȫʵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ���� | ���� |
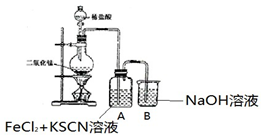 | I��A ����Һ��� ���Ժ���Һ�ɺ�ɫ��Ϊ��ɫ |
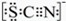
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬλ�� | B�� | ͬϵ�� | C�� | ͬ���칹�� | D�� | ͬ�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com