
【题目】以氯化氢为原料通过直接氧化法可以制取氯气,反应方程式为:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) 。
(1)该法可按下列催化过程进行:
CuCl2(s)CuCl(s)+![]() Cl2(g) ΔH1=83 kJ·mol-1
Cl2(g) ΔH1=83 kJ·mol-1
CuCl(s)+![]() O2(g)CuO(s)+
O2(g)CuO(s)+![]() Cl2(g) ΔH2=-20 kJ·mol-1
Cl2(g) ΔH2=-20 kJ·mol-1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=-121 kJ·mol-1
①总反应4HCl(g)+O2(g)2Cl2(g)+2H2O(g)的ΔH=____kJ·mol-1。
②有利于提高总反应平衡产率的条件有______。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)恒温恒压下,可以说明总反应4HCl(g)+O2(g)2Cl2(g)+2H2O(g)达到平衡的是_________。
A.压强不变
B.氯气的体积分数保持不变
C.每生成2个H—O的同时,有4个H—Cl生成
D.反应速率v正(O2)∶v逆(H2O)=1∶2
E.各组分的物质的量浓度都相等

(3)密闭容器中充入HCl和O2进行反应,c(HCl)随时间t的变化曲线如图1,保持其他条件不变,t2时升温,t3时重新达平衡,画出t2—t4时c(Cl2)随时间t的变化曲线____。
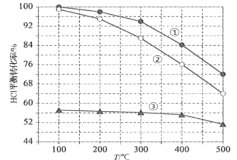
(4)在刚性容器中,进料浓度比c(HCl) ∶c(O2)分别等于1∶1、4∶1、7∶1时,HCl平衡转化率随温度变化的关系如图2:
①其中曲线①代表的c(HCl) ∶c(O2)是__________,原因__________。
②设HCl初始浓度为c0,根据进料浓度比c(HCl)∶c(O2)=4∶1的数据计算K(400℃)=__________(列出计算式,不必算出结果)。
【答案】-116 AD BD 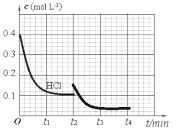 1∶1 温度不变,增大氧气浓度,HCl的平衡转化率增大
1∶1 温度不变,增大氧气浓度,HCl的平衡转化率增大 ![]()
【解析】
(1)①根据盖斯定律分析计算;②根据反应的焓变和气体分子数变化结合化学平衡移动的原理选择适合的反应条件;
(2) 根据化学平衡的特征分析判断;
(3)根据图1可知,起始时c(HCl)=0.4mol/L,平衡时,c(HCl)=0.1mol/L,则平衡时c(Cl2)= 0.15mol/L,保持其他条件不变,t2时升温,平衡逆向移动,达到新平衡时c(Cl2)减小,据此画出t2—t4时c(Cl2)随时间t的变化曲线;
(4)①根据图知,温度一定时进料浓度比c(HCl)∶c(O2)越小,HCl的转化率越大,据此分析判断进料浓度比c(HCl)∶c(O2)=1∶1时HCl的转化率曲线;②400℃时,进料浓度比c(HCl)∶c(O2)=4∶1的HCl转化率为76%,根据三段式计算解答。
(1)①i.CuCl2(s) CuCl(s)+ ![]() Cl2(g) △H1=83kJmol-1,ii.CuCl(s)+
Cl2(g) △H1=83kJmol-1,ii.CuCl(s)+ ![]() O2(g) CuO(s)+
O2(g) CuO(s)+ ![]() Cl2(g) △H2=-20kJmol-1,iii.CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) △H3=-121kJmol-1,根据盖斯定律,(i+ii+iii)×2可得:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) △H=[(83kJmol-1)+( -20kJmol-1)+( -121kJmol-1)]×2=-116kJmol-1,故答案为:-116;
Cl2(g) △H2=-20kJmol-1,iii.CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) △H3=-121kJmol-1,根据盖斯定律,(i+ii+iii)×2可得:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) △H=[(83kJmol-1)+( -20kJmol-1)+( -121kJmol-1)]×2=-116kJmol-1,故答案为:-116;
②总反应为4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) △H=-116kJmol-1,由勒夏特列原理可知,为了提高平衡产率,即平衡需要正向移动,低温和高压符合条件,故答案为:AD;
(2) A.恒温恒压下,压强始终不变,不能判断是平衡状态,故A错误;B.氯气的体积分数保持不变,说明反应达到了平衡状态,故B正确;C.根据方程式4HCl(g)+O2(g) 2Cl2(g)+2H2O(g),生成2个H—O,即生成1个水分子,4个H—Cl生成,即生成4个HCl分子,因此每生成2个H—O的同时,有4个H—Cl生成,说明正、逆反应速率不相等,不是平衡状态,故C错误;D.反应速率v正(O2)∶v逆(H2O)=1∶2,表示正逆反应速率相等,是平衡状态,故D正确;E.各组分的物质的量浓度都相等,不能说明各组分的物质的量浓度是否不变,不能判断是平衡状态,故E错误;故答案为:BD;
(3)根据 4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) △H=-116kJmol-1,结合图1可知,起始时c(HCl)=0.4mol/L,平衡时,c(HCl)=0.1mol/L,则平衡时c(Cl2)= 0.15mol/L,保持其他条件不变,t2时升温,平衡逆向移动,达到新平衡时c(Cl2)减小,t2—t4时c(Cl2)随时间t的变化曲线大致为 ,故答案为:
,故答案为: ;
;
(4)①根据图象,温度一定时,进料浓度比c(HCl)∶c(O2)越小,即增大氧气浓度,HCl的转化率增大,所以进料浓度比c(HCl)∶c(O2)=1∶1时,HCl的转化率在1∶
②400℃时,进料浓度比c(HCl)∶c(O2)=4∶1的HCl转化率为76%,
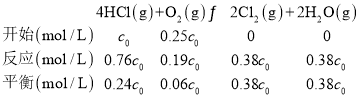
化学平衡常数K=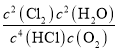 =
=![]() ,故答案为:
,故答案为:![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】磷酸铁(FePO42H2O,难溶于水的米白色固体)可用于生成药物、食品添加剂和锂离子电池的正极材料,实验室可通过下列实验制备磷酸铁.
(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤.反应加热的目的是_____.
(2)向滤液中加入一定量H2O2氧化Fe2+,为使滤液中的Fe2+完全被H2O2氧化成Fe3+,下列实验条件控制正确的是_____(填字母编号).
A.加入适当过量的H2O2溶液 B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行 D.用氨水调节溶液pH=7
(3)往含有Fe3+的溶液中加入一定量的Na2HPO4溶液(溶液显碱性),搅拌、过滤、洗漆、干燥得到FePO42H2O.若反应得到的FePO42H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为_____.
(4)实验过程中用H2O2氧化Fe2+之前,为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,离子方程式为:CrO![]() +6Fe2++14H+═2Cr3++6Fe3++7H2O
+6Fe2++14H+═2Cr3++6Fe3++7H2O
①在向滴定管注入K2Cr2O7标准溶液前,滴定管需要检漏、_____和_____.
②若滴定x mL含Fe2+的滤液消耗a molL﹣1K2Cr2O7标准溶液b mL,则滤液中c(Fe2+)=_____ molL﹣1.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硫酸亚铁晶体步骤如下:取洁净铁屑于烧杯中,加入一定量的稀硫酸,在50℃水浴中加热一段时间,趁热过滤,滤液转移至锥形瓶中,置于冰水浴中冷却,经一系列操作后获得产品。下列说法不正确的是( )
A.反应过程中烧杯底部一般保留少量铁屑以提高产品纯度
B.硫酸溶液浓度过低会降低晶体产率
C.水浴加热可以加快反应速率同时避免生成的![]() 发生爆炸
发生爆炸
D.与室温冷却相比,冰水浴冷却滤液可以更快获得更多更大的晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ· mol-1,下列说法或热化学方程式正确的是
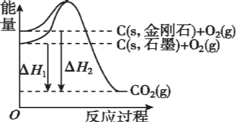
A.C(s,石墨)=C(s,金刚石) ΔH=+1.9 kJ· mol-1
B.拆开1mol金刚石和1mol O2中的化学键需要吸收395.4kJ的热量
C.金刚石的稳定性强于石墨
D.石墨的总键能比金刚石的总键能小1.9 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.MCl2在水溶液中的电离方程式为:MCl2=M2++2Cl,则M(OH)2可能是弱电解质
B.足量的锌分别与等体积、等pH的盐酸和醋酸反应,相同条件下产生氢气体积相同
C.已知,H2A=H++HA,HAH++A2,则NaHA溶液呈酸性
D.相同温度下,pH相等的氨水和氢氧化钠溶液中,c(NH![]() )=c(Na+)
)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业,是难溶于水的白色固体,能溶解于硝酸,在潮湿空气中可被迅速氧化。
Ⅰ.实验室用CuSO4—NaCl混合液与Na2SO3溶液反应制取CuCl。相关装置及数据如图:
图甲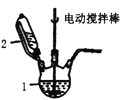 图乙
图乙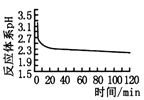 图丙
图丙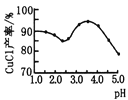
回答以下问题:
(1)甲图中仪器1的名称是________;制备过程中Na2SO3过量会发生副反应生成[Cu(SO3)2]3-,为提高产率,仪器2中所加试剂应为_____________。
(2)乙图是体系pH随时间变化关系图,写出制备CuCl的离子方程式_____________。丙图是产率随pH变化关系图,实验过程中往往用Na2SO3—Na2CO3混合溶液代替Na2SO3溶液,其中Na2CO3的作用是_______并维持pH在______左右以保证较高产率。
(3)反应完成后经抽滤、洗涤、干燥获得产品。洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是________。
Ⅱ.工业上常用CuCl作O2、CO的吸收剂,某同学利用如图所示装置模拟工业上测定高炉煤气中CO、CO2、N2和O2的含量。
A. 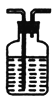 CuCl的盐酸溶液 B.
CuCl的盐酸溶液 B.  Na2S2O4和KOH的混合溶液
Na2S2O4和KOH的混合溶液
C.  KOH溶液 D.
KOH溶液 D. 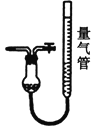
已知:Na2S2O4和KOH的混合溶液可吸收氧气。
(4)装置A中用盐酸而不能用硝酸,其原因是__________(用化学方程式表示)。用D装置测N2含量,读数时应注意________。整套实验装置的连接顺序应为_______________→D。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳的同素异形体有很多,我国科学家成功地合成了通过理论计算预言的T-碳。回答下列问题:
(1)基态碳原子价层电子的轨道表达式(电子排布图)为________。
(2)石墨炔可由六炔基苯![]() 在铜片的催化作用下发生偶联反应得到。
在铜片的催化作用下发生偶联反应得到。
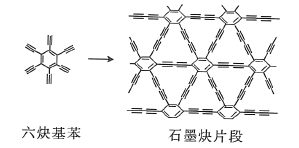
六炔基苯分子中的所有原子________(填“能”或“不能”)处于同一平面,六炔基苯属于________(填“极性”或“非极性”)分子,1个六炔基苯分子中含有![]() 键的数目为________。
键的数目为________。
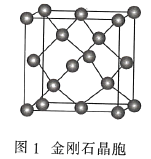
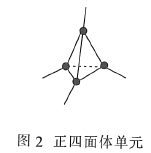
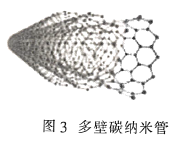
(3)金刚石(图1)中的每个碳原子用一个由4个碳原子组成的正四面体的结构单元(图2)取代,即得到T-碳。T-碳可通过皮秒激光照射悬浮在甲醇溶液中的多壁碳纳米管(图3)制得。多壁碳纳米管和T-碳中碳原子的杂化方式依次为________、________;溶剂甲醇中三种元素的电负性由大到小的顺序为________(用元素符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知辉铜矿、软锰矿的主要成分如下表所示:
矿石 | 辉铜矿 | 软锰矿 |
主要成分 | Cu2S、Fe2O3、SiO2 | MnO2、SiO2 |
某化工厂拟以这两种矿石为原料采用湿法冶炼铜,工艺如下:
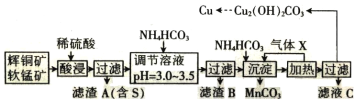
回答下列问题:
(1)气体 X 遇浓硝酸产生“白烟”,写出气体 X 的电子式:______________________________。
(2)提高“酸浸”速率的措施有______________________________(填两条)。
(3)用离子方程式表示“酸浸”中 MnO2 的作用:______________________________,被氧化的元素是______________________________(填元素符号)。
(4)已知 CH3COONH4 溶液呈中性,则常温下,NH4HCO3 溶液 pH______________________________(填“>”、“<”或“=”)7,理由是__________。
(5)从滤液 C 中可以提取一种化学肥料,它的化学式为_____________________________。
(6) 从溶液中析出的碱式碳酸铜可能带有结晶水,设其通式为 Cu2(OH)2CO3·xH2O。准确称取a g 样品,灼烧至恒重,称得 CuO 的质量,固体质量减轻 b g,则 x 为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2、碳酸盐、有机物等均是自然界碳循环中的重要物质。回答下列问题:
(1)下列物质属于化合物但不属于电解质的是______(填字母)。
A.石墨 B.汽油 C.乙醇 D.碳酸
(2)倍半碳酸钠(Na2CO3·NaHCO3·2H2O)在水溶液中的电离方程式为__________________________。
(3)金属钠在足量CO2中燃烧生成常见的盐和单质,写出反应的化学方程式:____________。
(4)铜器表面的难溶物Cu2(OH)2CO3可用稀硫酸洗涤除去,该反应的离子方程式为________________。
(5)工业上制取金刚砂的反应为: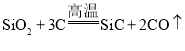 ,该反应中氧化剂与还原剂的物质的量之比为______。
,该反应中氧化剂与还原剂的物质的量之比为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com