
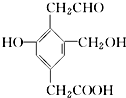
 某有机物X的结构简式如图所示.若1mol X分别与H2、Na、NaOH、NaHCO3恰好完全反应,则消耗H2、Na、NaOH、NaHCO3的物质的量之比为( )
某有机物X的结构简式如图所示.若1mol X分别与H2、Na、NaOH、NaHCO3恰好完全反应,则消耗H2、Na、NaOH、NaHCO3的物质的量之比为( )| A. | 4:3:2:1 | B. | 3:3:2:1 | C. | 4:3:2:2 | D. | 3:3:2:2 |
分析 该有机物中含有酚羟基、醛基、羧基和醇羟基、苯环,一定条件下,能和氢气反应的有苯环和醛基,能和氢氧化钠反应的有酚羟基和羧基,能和碳酸氢钠反应的只有羧基,酚羟基、羧基、醇羟基都能和钠反应,据此分析解答.
解答 解:该有机物中含有酚羟基、醛基、羧基和醇羟基、苯环,一定条件下,能和氢气反应的有苯环和醛基,能和氢氧化钠反应的有酚羟基和羧基,能和碳酸氢钠反应的只有羧基,所以若1mol X分别与H2、Na、NaOH、NaHCO3恰好完全反应,酚羟基、醇羟基、羧基能都能钠反应生成氢气,则消耗H2、Na、NaOH、NaHCO3的物质的量分别为4mol:3mol:2mol:1mol,故选A.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,注意酚羟基能和碳酸钠反应但和碳酸氢钠不反应,题目难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 蒸馏法是用海水制备淡水的主要方法之一 | |
| B. | 将饱和FeCl3溶液滴入到沸腾的蒸馏水中制备Fe(OH)3胶体 | |
| C. | 将氯气通入到热的氢氧化钠浓溶液中制备漂白液 | |
| D. | 用油脂的碱性水解反应制取肥皂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二者不反应,漂白性不变 | B. | 二者发生反应,漂白性增强 | ||
| C. | 二者发生反应,漂白性几乎消失 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸氢铵和氢氧化钠等物质的量混合 NH4++OH-═NH3↑+H2O | |
| B. | 向Ba(OH)2溶液中加入少量NaHSO3溶液 2HSO3-+Ba2++2OH-═BaSO3↓+SO32-+2H2O | |
| C. | 将Fe2O3溶于氢碘酸中Fe2O3+6H+═2Fe3++3H2O | |
| D. | 等物质的量的溴化亚铁跟氯气反应2Fe2++2Br-+2Cl2═2F3++Br2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| $\frac{c(HC{{O}_{3}}^{-})}{c({H}_{2}C{O}_{3})}$ | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
| A. | pH=7的血液中,c(HCO3-)=c(H2CO3) | |
| B. | 正常体温下人体发生碱中毒时,c(H+)•c(OH-)变大 | |
| C. | 人体发生酸中毒时,可静脉滴注一定浓度的NaHCO3溶液解毒 | |
| D. | $\frac{c(HC{{O}_{3}}^{-})}{c({H}_{2}C{O}_{3})}$=20.0时,H2CO3的电离程度大于HCO3-的水解程度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com