
关于化学平衡常数的叙述正确的是( )
A.温度一定,一个化学反应的平衡常数与反应物浓度成正比
B.两种物质反应,不管怎样书写化学方程式,平衡常数不变
C.温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数
D.浓度商Q<K,v正<v逆
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
体育比赛中,当运动员扭伤或肌肉挫伤时,队医随即对准运动员的受伤处喷射一氯乙烷(沸点12.27 ℃)进入局部冷冻麻醉处理。在一定条件下乙烯和氯化氢制取一氯乙烷的化学方程式为(有机物用结构简式表示)_____________________________________,该反应的类型是________________,决定一氯乙烷用于冷冻麻醉处理的具体性质是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
( )。
A.不管什么反应使用催化剂,都可以加快反应速率
B.可逆反应A(g)  B(g)+C(g),增大压强正反应速率和逆反应速率增大
B(g)+C(g),增大压强正反应速率和逆反应速率增大
C.对达到平衡的一个放热的可逆反应,若降低温度正反应速率减小,逆反应速率增大
D.参加反应物质的性质是决定化学反应速率的主要因素
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出表示含有8个质子,10个中子的原子的化学符号________;
(2)已知阴离子aX2-和阳离子bYn+具有相同的核外电子排布,则a、b、n之间的关系为a=________;
(3)比较下列大小(填“>”或“<”)
A.原子半径:Cl______Na
B.酸性:H2CO3______H2SiO3
(4)某元素R气态氢化物的化学式为RH3,其最高价氧化物中含氧量为,已知该元素的原子核中中子数和质子数相等,则该元素的名称是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应A+B—→C,如果温度每升高10 ℃,反应速率增加为原来的3倍。在10 ℃时,完成反应的20%需要54 min;将温度提高到40 ℃,完成反应的20%需要的时间为( )
A.2 min B.3 min
C.6 min D.9 min
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应2AB+D在四种不同的条件下进行,B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表。
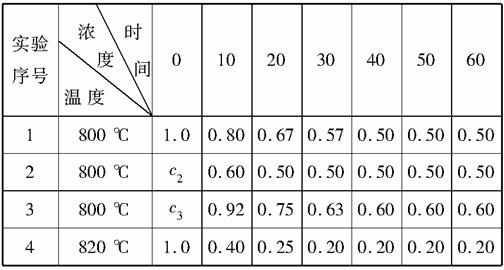
据上表,回答下列问题。
(1)在实验1中,反应物A在10~20分钟时间内平均速率为________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=________mol·L-1,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_________________
____________________________________________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3______(填“>”、“=”或“<”,下同)v1,且c3________1.0 mol·L-1。
(4)比较实验4和实验1,可推测该反应是________反应(填“吸热”、“放热”)。理由是___________________________________
_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应2AB+D在四种不同的条件下进行,B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表。
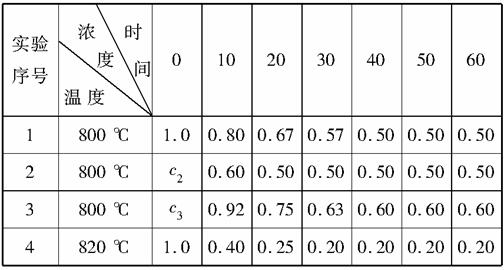
据上表,回答下列问题。
(1)在实验1中,反应物A在10~20分钟时间内平均速率为________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=________mol·L-1,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_________________
____________________________________________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3______(填“>”、“=”或“<”,下同)v1,且c3________1.0 mol·L-1。
(4)比较实验4和实验1,可推测该反应是________反应(填“吸热”、“放热”)。理由是___________________________________
_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组的同学们按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。
FeCl3+3H2O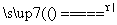 Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
(1)判断胶体制备是否成功,可利用胶体的_____________________________。
(2)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到________________,其原因是___________________。
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会_______________,原因是___________________________________________________________。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会__________________________________,原因是_____________________。
(3)丁同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是________________________________________。
②随后沉淀溶解,此反应的离子方程式是______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com