
| 实验 编号 | 试管1中的试剂 | 试管2中试剂 | 测得有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL 18mol/L浓硫酸 | 饱和Na2CO3碳酸钠溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol/L硫酸 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
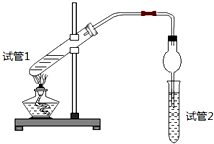 (1)写出实验A中试管1反应的化学方程式CH3COOH+C2H5OH
(1)写出实验A中试管1反应的化学方程式CH3COOH+C2H5OH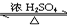 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.分析 (1)根据酯化反应原理可知,羧酸脱去羟基醇脱氢;
(2)对比试验关键是要采用控制变量,即控制一个变量,其它条件不变,所以可以从控制变量的角度来分析解答;
(3)根据实验A和实验B的数据进行解答;水在酯化反应中为生成物,从生成物对化学平衡的影响角度分析
(4)乙酸和乙醇容易挥发,且温度过高容易发生副反应.
解答 解:(1)由于酯化反应中,羧酸脱去的是羟基,醇脱去氢原子,生成乙酸乙酯和水,其反应方程式为CH3COOH+C2H5OH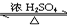 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
故答案为:CH3COOH+C2H5OH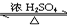 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(2)本题是研究实验D与实验C相对照,证明H+对酯化反应具有催化作用的条件,题中采用了一个变量,实验C3mol•L-1 H2SO4,实验D盐酸,所以达到实验目的,实验D与实验C中H+的浓度一样,实验C3mL乙醇、2mL乙酸、3mol•L-1 H2SO4,实验D3mL乙醇、2mL乙酸、盐酸,要保证溶液体积一致,才能保证乙醇、乙酸的浓度不变,盐酸体积为6mL,实验D与实验C中H+的浓度一样,所以盐酸的浓度为6mol•L-1,
故答案为:6,6;
(3)对照实验A和B可知:试管Ⅰ中试剂实验A比实验B多1mL18mol•L-1 浓硫酸,但是试管Ⅱ中试剂中测得有机层乙酸乙酯的厚度,实验A为5.0cm,而实验B只有0.1cm,说明浓硫酸的吸水性提高了乙酸乙酯的产率;酯化反应为可逆反应,浓硫酸吸收酯化反应生成的水,降低了生成物浓度,使平衡向生成乙酸乙酯方向移动,
故答案为:A;浓硫酸吸收酯化反应生成的水,降低了生成物浓度,使平衡向生成乙酸乙酯方向移动;
(4)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应,实验发现温度过高,乙酸乙酯的产率反而降低,是由于乙酸、乙醇都易挥发,使产率降低,或因温度过高可能发生副反应使产率降低,如乙醇在140℃,在浓硫酸催化下脱水生成乙醚,
故答案为:乙酸、乙醇都易挥发,温度过高可能使乙酸、乙醇大量挥发使产率降低,温度过高可能发生副反应使产率降低.
点评 本题考查了乙酸乙酯的制备方法、温度对反应速率、化学平衡的影响等知识,题目难度中等,注意把握乙酸乙酯的制备原理和实验方法,明确影响反应速率、化学平衡的因素.


科目:高中化学 来源: 题型:选择题
| A. | 1mol苯中含有3nA个碳碳双键 | |
| B. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 一定条件下2 mol SO2和1 mol O2充分反应后,混合气体的分子总数大于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HClO4<HBrO4<HIO4 | B. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | ||
| C. | 稳定性:HCl<H2S<PH3 | D. | 还原性:Cl->Br->I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4 C2H6 | B. | C2H4 C3H6 | C. | C2H4 C2H6O | D. | C2H6O C2H4O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 试剂 | 现象 | 结论 |
| A | 酸性KMnO4溶液 | 溶液褪色 | SO2有氧化性 |
| B | FeCl3溶液 | 溶液褪至浅绿色 | SO2有还原性 |
| C | 滴有酚酞的NaOH溶液 | 无明显变化 | SO2与NaOH溶液不反应 |
| D | 紫色石蕊试液 | 溶液变红后褪色 | SO2水溶液有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
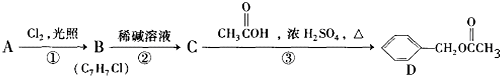
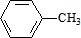 ,C的名称:苯甲醇
,C的名称:苯甲醇 +Cl2 $\stackrel{光照}{→}$
+Cl2 $\stackrel{光照}{→}$ 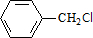 +HCl,取代反应
+HCl,取代反应 ,取代反应
,取代反应 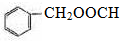 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
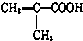 )$\stackrel{一定条件}{→}$PMAA
)$\stackrel{一定条件}{→}$PMAA .
. $→_{△}^{浓硫酸}$CH2=C(CH3)-COOH+H2O
$→_{△}^{浓硫酸}$CH2=C(CH3)-COOH+H2O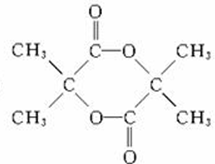 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com