
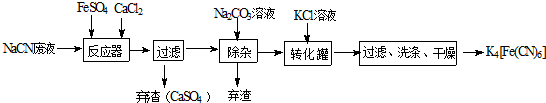
���� ��ʵ��Ŀ���Ǻϳɻ�Ѫ�Σ������̿�֪��NaCN��Һ�м��������������Ȼ��ƣ�����6NaCN+FeSO4+CaCl2=Na4[Fe��CN��6+CaSO4��+2NaCl��Ȼ�����̼������Һ�ɳ�ȥ������Ca2+�������˺�����Һ�м���KCl��ת������K4[Fe��CN��6��˵��K4[Fe��CN��6�ܽ�Ƚ�С���Դ˽����⣮
��1��NaCNΪǿ�������Σ���Һ��CN-����ˮ����Һ�ʼ��ԣ���������Һʱ����ˮ�⣬�ݴ˴��⣻
��2��NaCN��Һ�м��������������Ȼ��ƣ�����6NaCN+FeSO4+CaCl2=Na4[Fe��CN��6+CaSO4��+2NaCl��
��3����Ӧ���м����Ȼ��ƣ���Ҫ����̼���Ƴ�ȥ��
��4�������˺�����Һ�м���KCl��ת������K4[Fe��CN��6��˵��K4[Fe��CN��6�ܽ�Ƚ�С��
��5������ԭ���غ�͵����غ���ƽ��д��ѧ����ʽ��
��6��AgCl���Ѫ����ȡ���Һ�ɽ���ת��ΪK4[Ag2 ��CN��6]����ϵ绰�غ㣬ԭ���غ�����д��
��7������������ԭ��Ӧԭ�������õ��ӵ�ʧ�غ���������ص����ʵ�����
��� �⣺ʵ��Ŀ���Ǻϳɻ�Ѫ�Σ������̿�֪��NaCN��Һ�м��������������Ȼ��ƣ�����6NaCN+FeSO4+CaCl2=Na4[Fe��CN��6+CaSO4��+2NaCl��Ȼ�����̼������Һ�ɳ�ȥ������Ca2+�������˺�����Һ�м���KCl��ת������K4[Fe��CN��6��˵��K4[Fe��CN��6�ܽ�Ƚ�С��
��1��NaCNΪǿ�������Σ���Һ��CN-����ˮ����Һ�ʼ��ԣ�NaCNˮ��ʼ��Ե����ӷ���ʽΪ��CN-+H2O?HCN+OH-��Ϊ����ˮ�⣬��������Һʱ�ɽ����ܽ�������������Һ�У��ڼ�ˮϡ�ͣ�
�ʴ�Ϊ��NaOH��
��2��NaCN��Һ�м��������������Ȼ��ƣ�����6NaCN+FeSO4+CaCl2=Na4[Fe��CN��6+CaSO4��+2NaCl�����Լ���Fe3+�����ӷ���ʽΪ��K++[Fe��CN��6]4-+Fe3+=KFe[Fe��CN��6]��������Tl2SO4�ж��ķ���ʽΪKFe[Fe��CN��6]��s��+Tl+��aq��=TlFe[Fe��CN��6]��s��+K+��aq����
�ʴ�Ϊ��K++[Fe��CN��6]4-+Fe3+=KFe[Fe��CN��6]����KFe[Fe��CN��6]��s��+Tl+��aq��=TlFe[Fe��CN��6]��s��+K+��aq����
��3����Ӧ���м����Ȼ��ƣ�����̼������Һ�ɳ�ȥ������Ca2+��
�ʴ�Ϊ����ȥ���е�Ca2+��
��4�������˺�����Һ�м���KCl��ת������K4[Fe��CN��6��˵��K4[Fe��CN��6�ܽ�Ƚ�С��
�ʴ�Ϊ������
��5������K4Fe��CN��6��ϵ��Ϊ3�����ԭ���غ㣬Fe3Cǰϵ��Ϊ3��KCNǰϵ��Ϊ12�������غ�õ�N2ǰϵ��Ϊ1�����ݵ�ԭ���غ㣬��CN��2ǰϵ��Ϊ2��̼ԭ���غ㣬Cǰϵ��Ϊ1����ƽ�õ��Ļ�ѧ����ʽΪ��3K4Fe��CN��6=Fe3C+12KCN+N2��+C+2��CN��2����
�ʴ�Ϊ��12��1��1��2��1��
��6�����Һ����ֱ������������Һ���ɽ���ת��ΪK4[Ag2 ��CN��6]��AgCl���Ѫ����ȡ���Һ�ɽ���ת��ΪK4[Ag2 ��CN��6]����Ӧ�����ӷ���ʽΪ��2AgCl+[Fe��CN��6]4-=Fe2++[Ag2 ��CN��6]4-+2Cl-��
�ʴ�Ϊ��2AgCl+[Fe��CN��6]4-=Fe2++[Ag2 ��CN��6]4-+2Cl-��
��7��1mol K4Fe��CN��6�������������ʱ��Fe���ϼ���+2�����ߵ�+3�ۣ�NԪ�ػ��ϼ���-3�����ߵ�+5�ۣ�CԪ�ػ��ϼ���+2�����ߵ�+4�ۣ���Fe��N��C�Ļ��ϼ�������1+6����8+2��=61�ۣ���ʧȥ61mol���ӣ�����������е���Ԫ�ش�+7��Ϊ+2�ۣ���õ�5mol���ӣ����ݵ����غ㣬1mol K4Fe��CN��6��������������������ĸ�����ص����ʵ���Ϊ12.2mool��
�ʴ�Ϊ��12.2��
���� ���⿼�����ʵ��Ʊ�ʵ�鷽������ƣ�������ѧ���ķ���������ʵ�������ͼ��������Ŀ��飬Ϊ�߿��������ͣ�ע���������ͼ����ʵ���ԭ���Ͳ����������Ѷ��еȣ�ע�����������ԭ��Ӧ�Ļ��ϼ۵�����������ȼ��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢܢޢ� | B�� | �٢ڢۢ� | C�� | �٢ۢܢݢ� | D�� | �ۢܢݢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| �� | �� | �� | ||||||
| �� | �� | �� | �� | �� | �� | �� | �� | |
| �� | �� | ⑪ | ⑫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.15mol/��L•min�� | B�� | 0.3mol/��L•min�� | C�� | 0.45mol/��L•min�� | D�� | 0.6mol/��L•min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡH2SO4 | B�� | ����������Һ | C�� | ����ͭ��Һ | D�� | �Ȼ�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ʵ����ʵ | ���ۻ���� | |
| A | ��ij��Һ�еμ���ˮ�����Ȼ�̼�����ú�ֲ㣬���Ȼ�̼���Ϻ�ɫ | ˵��ԭ��Һ�к���I- |
| B | ��SO2��ˮ��Һ�еμ����ᱵ��Һ�а�ɫ���� | ���ɵij���ΪBaSO3 |
| C | ��FeSO4��Һ�еμ����Ը��������Һ�����������Һ��ɫ | Fe2+���л�ԭ�� |
| D | 25�������ᱵ������Һ�м��������������ƹ��壬�����ᱵ�������� | ����c��SO42-����Ksp��BaSO4����С |
| A�� | A�� | B�� | B�� | C�� | C�� | D�� | D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ��ѧ�� | H-H | C-O | H-O | C-H |
| E/��kJ•mol-1�� | 436 | 343 | 465 | 413 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com