
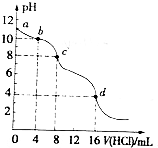
 用已知浓度的盐酸滴定未知浓度的Na2CO3溶液.测得混合溶液的pH随所加盐酸体积的变化曲线如图(已知饱和CO2溶液pH为3.9),下列说法正确的是( )
用已知浓度的盐酸滴定未知浓度的Na2CO3溶液.测得混合溶液的pH随所加盐酸体积的变化曲线如图(已知饱和CO2溶液pH为3.9),下列说法正确的是( )| A. | 该Na2CO3溶液的浓度为0.001mol/L | |
| B. | pH=6时,c(Na+)>c(HCO3-)>c(CO32-) | |
| C. | 在pH=7时,c(Na+)=c(Cl-) | |
| D. | c→d发生的主要离子反应为:CO32-+H+=HCO3- |
分析 A、根据滴定之前溶液的pH来计算碳酸钠的浓度;
B、在pH=6时,溶液显酸性,根据溶液的组成情况确定离子浓度的大小关系;
C、根据电荷守恒以及溶液显示中性时氢离子和氢氧根离子浓度相等来判断;
D、根据pH变化图象结合滴定实际来回答.
解答 解:A、滴定之前碳酸钠溶液的pH=11,所以溶液中氢氧根离子的浓度为0.001 mol•L-1,该Na2CO3溶液的浓度大于0.001 mol•L-1,故A错误;
B、在pH=6时,溶液显酸性,溶液的组成是:碳酸和碳酸钠溶液的混合物,故此时c(Na+)>c(HCO3-)>c(CO32-),故B正确;
C、在pH=7时,溶液显示中性,氢离子和氢氧根离子浓度相等,此时溶液中还含有碳酸根离子和碳酸氢根离子,所以钠离子大于氯离子浓度,故C错误;
D、根据pH变化曲线,可以看出c到d阶段,随着盐酸的加入,pH不再变化,所以该阶段盐酸剩余,碳酸钠和碳酸氢钠完全消耗掉了,故D错误.
故选B.
点评 本题综合考查离子浓度的大小比较,题目难度较大,本题注意分析反应物的物质的量之间的关系,判断反应的程度以及溶液的主要成分是解题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 有机物分子结构十分复杂 | |
| B. | 自然界中存在着多种形式的大量的有机物 | |
| C. | 碳原子能与其他原子形成四个共价键,且碳原子间也可以成键,而且有同分异构现象 | |
| D. | 有机物除含碳元素之外,还含有其他多种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使酸性KMnO4溶液褪色的反应 | B. | 甲烷与氯气在光照条件下的反应 | ||
| C. | 乙烯使溴水褪色的反应 | D. | 乙烯的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小于200mL | B. | 200mL | C. | 大于200mL | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COO-的浓度基本不变 | |
| B. | SO${\;}_{3}^{2-}$的浓度减小,而SO${\;}_{4}^{2-}$的浓度增大 | |
| C. | CO${\;}_{3}^{2-}$的浓度减小,溶液碱性增强 | |
| D. | HCO${\;}_{3}^{-}$的浓度减,OH-的浓度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3Cl2+6NaOH=2NaClO3+5NaCl+3H2O | |
| B. | CaH2+2H2O=Ca(OH)2+2H2↑ | |
| C. | AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl | |
| D. | 2CuO+Cu2S=4Cu+SO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 由不同原子组成的纯净物一定是化合物 | |
| B. | 一定温度和压强下,30 L某种气态纯净物中含有6.02×1023个分子,这些分子由1.204×1024个原子组成,则该气体中每个分子含有2个原子 | |
| C. | 含金属元素的离子一定都是阳离子 | |
| D. | 胆矾是混净物,水泥是混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 、CH 3COOH、HCl的排列中,
、CH 3COOH、HCl的排列中, 应填入的物质是( )
应填入的物质是( )| A. | H2SO4 | B. | CH3CH2OH | C. | H2CO3 | D. | CH3COOCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往新配制的可溶性淀粉溶液中滴加碘水,溶液显蓝色,用CCl4不能从中萃取出碘 | |
| B. | 当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 | |
| C. | 蒸馏操作时,温度计水银球的位置应在蒸馏烧瓶的支管口处 | |
| D. | 提取海带中碘元素时,为保证I-完全氧化为I2,加入的氧化剂(H2O2或新制氯水)均应过量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com