

分析 甲、乙均是离子化合物,且阴、阳离子个数比为1:1,甲可作发酵粉,则甲为NaHCO3,A为Na2CO3,乙是一种常用的化肥,由图中转化关系可知,乙为NH4HCO3,则B为CO2,D为NH3,C为H2O,以此解答该题.
解答 解:甲、乙均是离子化合物,且阴、阳离子个数比为1:1,甲可作发酵粉,则甲为NaHCO3,A为Na2CO3,乙是一种常用的化肥,由图中转化关系可知,乙为NH4HCO3,则B为CO2,D为NH3,C为H2O.
(1)由以上分析,可知甲为NaHCO3,俗名小苏打,故答案为:小苏打;
(2)D为NH3,溶于水生成的NH3•H2O为溶解,发生电离NH3•H2O=NH4++OH-,溶液显碱性,加入酚酞后溶液显红色,
故答案为:碱性;D为NH3,溶于水生成的NH3•H2O为溶解,发生电离NH3•H2O=NH4++OH-;
(3)乙为NH4HCO3,与过量的KOH溶液共热,反应的离子方程式:NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$CO32-+NH3↑+2H2O,故答案为:NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$CO32-+NH3↑+2H2O.
点评 本题考查无机物的推断,注意根据物质的用途、组成及分解反应等进行推断,需要学生熟练掌握元素化合物知识,难度中等.


科目:高中化学 来源: 题型:填空题
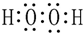
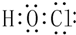
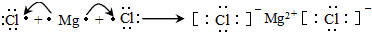
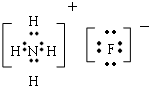
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的密度不再改变的状态 | |
| B. | 单位时间生成2n mol C,同时生成n mol D | |
| C. | 混合气体的压强不再改变的状态 | |
| D. | A、B、C、D的分子数之比为1:3:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 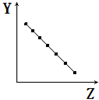 表示第三周期元素的原子半径(稀有气体除外) | |
| B. | 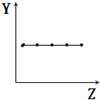 表示ⅡA族元素的最外层电子数 | |
| C. | 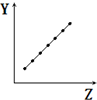 表示第二周期元素的电负性(稀有气体除外) | |
| D. | 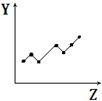 表示第三周期元素的第一电离能(稀有气体除外) | |
| E. | 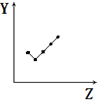 表示第ⅦA族元素氢化物的沸点. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
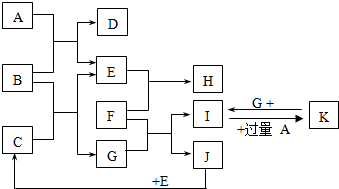 如图为一些常见物质间的相互转化关系,其中F为金属,高温下能与某些金属氧化物反应,是工业冶炼金属的方法之一. A为无色气体,B为淡黄色固体,C为无色液体,E和J为无色气体单质.
如图为一些常见物质间的相互转化关系,其中F为金属,高温下能与某些金属氧化物反应,是工业冶炼金属的方法之一. A为无色气体,B为淡黄色固体,C为无色液体,E和J为无色气体单质.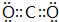 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 研制乙醇汽油(汽油中添加一定比例乙醇)技术,不能降低机动车尾气中有害气体排放 | |
| B. | 工业上用石灰乳对煤燃烧后形成的烟气进行脱硫,最终能制得石膏 | |
| C. | 为了有效的发展清洁能源,采用电解水的方法大量制备H2 | |
| D. | 世博停车场安装催化光解设施,可将汽车尾气中CO和NOx反应生成无毒气体 | |
| E. | 利用化学反应原理,设计和制造新的药物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,该烯烃的结构简式和名称为CH3CH═CHCH(CH3)CH2CH═CHCH2CH3,4-甲基-2,7-壬二烯.
,该烯烃的结构简式和名称为CH3CH═CHCH(CH3)CH2CH═CHCH2CH3,4-甲基-2,7-壬二烯.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/min | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com