
| A、铝热剂就是单指Fe2O3和铝粉的混合物 |
| B、检验红色物质是否是Fe2O3的操作步骤为:样品-→粉碎-→加水溶解-→过滤-→向滤液中滴加KSCN溶液 |
| C、分别还原a mol Fe2O3所需提供的H2、Al、CO的物质的量之比为3:2:3 |
| D、明矾属硫酸盐,含结晶水,是纯净物 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯、水、四氯化碳三种无色液体不用试剂就可以鉴别开来 |
| B、甘氨酸既能与HCl反应又能与NaOH反应,所以甘氨酸是两性氧化物 |
| C、检验淀粉是否已完全水解,只需要向水解混合液中加银氨溶液并水浴加热即可 |
| D、等质量的C3H6、C4H10、C6H6完全燃烧,耗氧最多的是C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加适量浓硫酸、微热、蒸发 |
| B、加适量稀硫酸、微热、过滤 |
| C、加适量水、微热、蒸发 |
| D、加适量稀硫酸、微热、蒸发 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
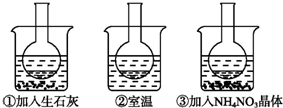 如图所示三个烧瓶中分别装入含酚酞的0.01mol?L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,烧杯②中不加任何物质,向烧杯③中加入NH4NO3晶体.
如图所示三个烧瓶中分别装入含酚酞的0.01mol?L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,烧杯②中不加任何物质,向烧杯③中加入NH4NO3晶体.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④ | C、①④ | D、②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com