
【题目】(1)根据分子中所含官能团可预测有机化合物的性质。
①下列化合物中,能与H2发生加成反应的是______(填字母)。
a.CH3Cl b.CH≡CH c.CH3CH2OH
②下列化合物中,能与NaHCO3发生反应的是______(填字母)。
a.CH3CH2OH b.CH3CHO c.CH3COOH
③下列化合物中,遇到FeCl3溶液显紫色的是______(填字母)。
a.![]() b.
b.![]() c.
c.![]()
(2)甲基丙烯酸甲酯(![]() )是合成有机玻璃的单体。
)是合成有机玻璃的单体。
①1 mol甲基丙烯酸甲酯最多与______ mol H2发生反应。
②写出甲基丙烯酸甲酯在酸性条件下水解的化学方程式:______。
③有机玻璃可由甲基丙烯酸甲酯通过加聚反应得到,有机玻璃的结构简式为______。
(3)水杨醛是一种天然香料的中间体,可通过下列方法合成:

①B中官能团的名称为______和______。
②A→B的反应类型为______。
③水杨醛的结构简式为______。
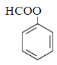
④水杨醛的同分异构体X能发生水解反应,且1 mol X最多能与2 mol NaOH反应。写出符合上述条件X的结构简式:______。
【答案】b c b 1mol ![]() +H2O
+H2O![]() CH2=C(CH3)COOH+CH3OH
CH2=C(CH3)COOH+CH3OH 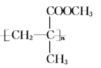 氯原子 酚羟基 取代反应
氯原子 酚羟基 取代反应 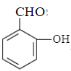
【解析】
(1)①CH3Cl、CH3CH2OH中均没有不饱和键,不能发生加成反应,CH≡CH含有碳碳三键,能与H2发生加成反应;
故答案为:b;
②CH3CH2OH、CH3CHO均不能电离产生氢离子,均不能与NaHCO3发生反应,CH3COOH可以电离出氢离子,使溶液显酸性,能与NaHCO3发生反应;
故答案为:c;
③![]() 遇到FeCl3溶液显紫色;
遇到FeCl3溶液显紫色;
故答案为:b;
(2)①![]() 分子中含有1个碳碳双键,能与H2发生加成反应,则1mol甲基丙烯酸甲酯最多与1mol H2发生反应;
分子中含有1个碳碳双键,能与H2发生加成反应,则1mol甲基丙烯酸甲酯最多与1mol H2发生反应;
故答案为:1mol;
②甲基丙烯酸甲酯在酸性条件下水解生成甲基丙烯酸和甲醇,反应的化学方程式为:![]() +H2O
+H2O![]() CH2=C(CH3)COOH+CH3OH;
CH2=C(CH3)COOH+CH3OH;
故答案为:![]() +H2O
+H2O![]() CH2=C(CH3)COOH+CH3OH;
CH2=C(CH3)COOH+CH3OH;
③甲基丙烯酸甲酯含有碳碳双键,碳碳双键可发生加聚反应,则有机玻璃的结构简式为 ;
;
故答案为: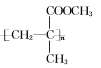 ;
;
(3)①由B的结构简式可知,B中官能团的名称为氯原子和酚羟基;
故答案为:氯原子;酚羟基;
②结合A、B的结构简式以及A→B的反应条件可知,A→B的反应为Cl原子取代了A甲基上的氢原子,则反应类型为取代反应;
故答案为:取代反应;
③B发生卤代烃的水解,且同一个碳原子上连接两个羟基时,不稳定,会脱去分子水引入CHO,酸化得到水杨醛,故水杨醛的结构简式为: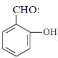 ;
;
故答案为: ;
;
④水杨醛的同分异构体X能发生水解反应,且1 mol X最多能与2 mol NaOH反应,则X中含有甲酸与酚形成的酯基,即取代基为-OOCH,故X的结构简式为:![]() ;
;
故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知用硫酸酸化的草酸(H2C2O4)溶液能与KMnO4溶液反应.某化学小组研究发现,少量MnSO4可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,探究不同的初始pH和草酸溶液浓度对反应速率的影响,设计如下实验,则A=____,C=____,E=_____.
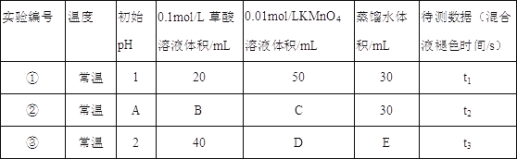
(2)该反应的离子方程式______________________________________.
(3)若t1<t2,则根据实验①和②得到的结论是_____________________________.
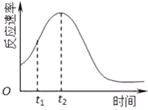
(4)小组同学发现每组实验反应速率随时间的变化总是如图,其中t1~t2时间内速率变快的主要原因可能是:①__________________;②__________________________.
(5)化学小组用滴定法测定KMnO4溶液物质的量浓度:取ag草酸晶体(H2C2O42H2O,摩尔质量126g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定三次,平均消耗KMnO4溶液VmL.滴定到达终点的现象是:______________________________;实验中所需的定量仪器有__________________(填仪器名称).该KMnO4溶液的物质的量浓度为____mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】位于短周期的四种主族元素A、B、C、D,原子序数依次增大,已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。E是自然界中含量最高的金属。根据你的推断完成下列问题:
(1)E元素在周期表中的位置为_______。
(2)写出由上述元素形成的具有漂白作用的三种物质的化学式_______。
(3)用电子式表示C与D形成化合物的过程_______。
(4)写出E的最高价氧化物与强碱反应的离子方程式________。
(5)B、C两元素形成的原子个数比为1:1的化合物中的化学键为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式为:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH= -890.3 kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用而产生的能量存活,甲烷细菌使1 mol甲烷生成CO2气体与液态水,放出的能量____________(填“>”、“<”或“=”)890.3 kJ。
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2= 2CO+2H2,1 g CH4完全反应可释放15.46 kJ的热量,则:

①上图(所有物质均为气态)能表示该反应过程中能量变化的是__________(填字母)。
②若将物质的量均为1 mol的CH4与CO2充入某恒容密闭容器中,体系放出的热量随时间的变化如图所示,则CH4的转化率为 。

(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)=CH4(g)的反应热无法直接测量,但通过上述反应可求出C(s)+2H2(g)=CH4(g)的反应热ΔH= 。
(4)目前对于上述三种物质的研究是燃料研究的重点,下列关于上述三种物质的研究方向中可行的是_____________(填字母)。
A.寻找优质催化剂,使CO2与H2O反应生成CH4与O2,并放出热量
B.将固态碳合成为C60,以C60作为燃料
C.寻找优质催化剂,利用太阳能使大气中的CO2与海底开采的CH4合成合成气(CO、H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,用0.1000mol/LNaOH溶液滴定25.00mL0.1000mol/L 某一元酸HX 溶液,滴定过程中pH变化曲线如图所示,下列说法不正确的是
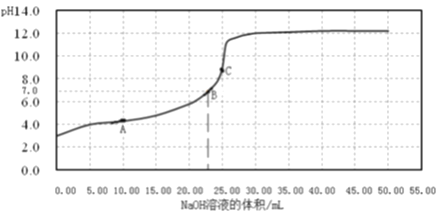
A. 在A点:c (HX)>c(Na+)>c(X-) B. 在B点,溶液中c(H+)=c(OH-)
C. 0.05mol/L NaX 溶液的pH≈9.0 D. C 点溶液中存在的主要平衡是X-+ H2O![]() HX+OH-
HX+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如下图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是:
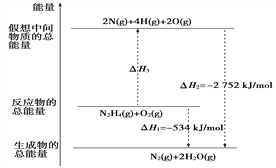
A. 194 B. 391 C. 516 D. 658
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学为探究H2O2、H2SO3、Br2的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
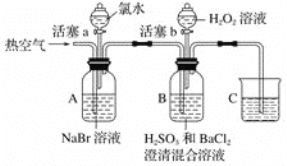
实验记录如下:
实验操作 | 实验现象 | |
Ⅰ | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为红棕色 |
Ⅱ | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
请回答下列问题:
(1)A中反应的离子方程式是______。
(2)实验操作Ⅱ吹入热空气的目的是_____。
(3)装置C的作用是_____,C中盛放的药品是_____。
(4)实验操作Ⅲ,混合液逐渐变成红棕色,其对应的离子方程式是_____。
(5)由上述实验得出的结论是______。
(6)实验反思:
①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是________。
②实验操作Ⅲ,开始时颜色无明显变化的原因是(写出一条即可)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程的示意图如图所示,下列说法正确的是
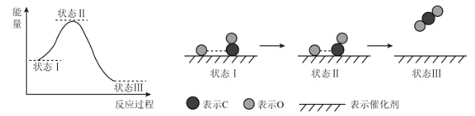
A.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
B.同物质的量的CO和O反应比CO与O2反应放出更多的热量
C.CO和O生成CO2是吸热反应
D.在该过程中,CO断键形成C和O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类中,所属关系不符合“X包含Y、Y包含Z”的有
选项 | X | Y | Z |
A | 芳香族化合物 | 芳香烃的衍生物 |
|
B | 脂肪族化合物 | 链状烃的衍生物 | CH3COOH(乙酸) |
C | 环状化合物 | 芳香族化合物 | 苯的同系物 |
D | 不饱和烃 | 芳香烃 |
|
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com