
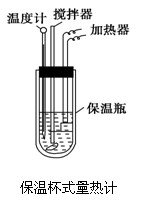


 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 SO3(g)+NO(g) �ﵽƽ�⣬����Ӧ������ʱ��仯����ͼ��ʾ������ȷ�Ľ�����
SO3(g)+NO(g) �ﵽƽ�⣬����Ӧ������ʱ��仯����ͼ��ʾ������ȷ�Ľ�����
| A���淴Ӧ���ʣ�a��С�ڵ�c |
| B����Ӧ��Ũ�ȣ�a��С�ڵ�b |
| C����Ӧ��c��ʱSO2��ת������� |
| D����Ӧ�������������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���Ȼ�ѧ����ʽδע���¶Ⱥ�ѹǿʱ����H��ʾ��״���µ����� |
| B���Ȼ�ѧ����ʽ�еĻ�ѧ������ֻ������Ӧ�������������ʵ��� |
| C���ڼ��������½��еķ�Ӧһ�������ȷ�Ӧ |
| D��ͬһ��ѧ��Ӧ��Ӧ������ͬ����Hֵһ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
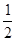 O2 ( g ) �� H2O ( g ) ��H1 =" a" kJ/mol
O2 ( g ) �� H2O ( g ) ��H1 =" a" kJ/mol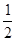 O2 ( g ) �� H2O ( l ) ��H3 =" c" kJ/mol
O2 ( g ) �� H2O ( l ) ��H3 =" c" kJ/mol| A��c<a<0 | B��b>d>0 | C��2a=b< 0 | D��2c=d>0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ƽ | B���¶ȼ� | C�����β�������� | D����Ͳ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
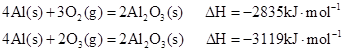
| A��O3��O2�ȶ�����O2ת��ΪO3�����ȷ�Ӧ |
| B��O2��O3�ȶ�����O2ת��ΪO3�Ƿ��ȷ�Ӧ |
| C����������O2��O3�����ߣ���O2ת��ΪO3�Ƿ��ȷ�Ӧ |
| D����������O2��O3�����ͣ���O2ת��ΪO3�����ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
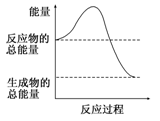
| A��H2O(g)===H2O(l)����H����44.0 kJ/mol |
| B��2HI(g)===H2(g)��I2(g)����H����14.9 kJ/mol |
| C���γɻ�ѧ��ʱ���ų�862 kJ�����Ļ�ѧ��Ӧ |
| D�������仯��ͼ��ʾ�Ļ�ѧ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ʹ¯����������ܽ�ʡȼ�� |
| B���䲻��ʹ¯������������Խ�ʡȼ�� |
| C�����ܽ�ʡȼ�ϣ�����ʹ¯��˲����� |
| D���Ȳ���ʹ¯��������ֲ��ܽ�ʡȼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����˻��ȼ����Ҫ�ǽ���ѧ��ת��Ϊ���ܺ��� |
B�����˻��ȼ�շ�Ӧ���̺������仯����ͼ��ʾ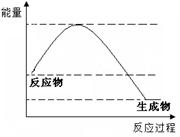 |
| C������ȼ�յ��Ȼ�ѧ����ʽΪ��C3H8(g) + 5O2(g)����3CO2(g)+ 4H20(g)����H=-2221��5 kJ��mol-1 |
| D�����顢��������Ƭ�����ȼ�ϵ�أ��ڱ��鸽���IJ���Ϊ��صĸ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com