
【题目】下面有关晶体的叙述中,不正确的是( )
A.金刚石为网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围紧邻且距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻且距离相等的Cl-有8个
D.干冰晶体中,每个CO2分子周围紧邻且距离相等的CO2分子有12个
【答案】B
【解析】
A.金刚石的晶胞结构如图所示: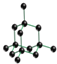 ,根据图可知由共价键形成的最小碳环上有6个碳原子,故A正确;
,根据图可知由共价键形成的最小碳环上有6个碳原子,故A正确;
B.氯化钠晶体中,钠离子在体心和棱心位置,氯离子在顶点和面心位置,1个钠离子与6个氯离子构成正八面体,所以每个钠离子与6个最近且等距离的氯离子以离子键结合,与每个氯离子最近的且等距离的氯离子有12个,故B错误;
C.氯化铯晶体晶胞结构如图: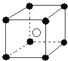 ,Cs+位于该晶胞的体心;而Cl-位于该晶胞的顶点,每个晶胞中含有一个铯离子,每个顶点上的氯离子被8个晶胞共用,每个氯离子周围最近的铯离子是8,故C正确;
,Cs+位于该晶胞的体心;而Cl-位于该晶胞的顶点,每个晶胞中含有一个铯离子,每个顶点上的氯离子被8个晶胞共用,每个氯离子周围最近的铯离子是8,故C正确;
D.二氧化碳晶体属于面心立方,采用沿X、Y、Z三轴切割的方法判断二氧化碳分子的个数为12,所以在CO2晶体中,与每个CO2分子周围紧邻的有12个CO2分子,故D正确;
答案选B。


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是( )
A.升温不利于正反应生成Ni(CO)4(g)
B.在25 ℃时,反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10-5
C.在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v正>v逆
D.在80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、镁、金等的相关物质在生产生活中具有重要的作用。回答下列问题:
(1)铜元素在周期表中的位置是___________,基态铜原子中,核外电子占据最高能层的符号是___________,占据该最高能层的电子数为___________。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、 Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于___________(填“晶体”或“非晶体”)
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,lmol(SCN)2分子中含有σ键的数目为___________。(SCN)2对应的酸有硫氰酸(H-S-C≡N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________________________。
(4)铜与金形成的金属互化物的晶胞结构如图1所示,其晶胞边长为anm,该金属互化物的密度为___________(用含a、NA的代数式表示)g·cm-3。

(6)某金属晶体中原子的堆积方式为六方最密堆积如图2所示,晶胞可用图3表示。已知该金属的原子半径为acm,该金属晶胞的高为bcm:若以晶胞中A点原子为原点建立空间直角坐标系o-xyz,则A点原子的坐标为(0,0,0),C点原子的坐标为(2a,0,0),D点原子的坐标为(0,0,b),则B点原子的坐标为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阳离子和一种阴离子且互不重复)。
阳离子 | K+、Na+、Ba2+、NH |
阴离子 | CH3COO-、Cl-、OH-、SO |
已知:①A、C溶液的pH均大于7,B溶液的pH小于7,A、B溶液中水的电离程度相同;D物质的焰色反应呈黄色;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成有刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A的名称是_______B的化学式_______
(2)写出C溶液和D溶液反应的化学方程式___________
(3)25 ℃时,pH=9的A溶液和pH=9的C溶液中水的电离程度小的是___(填A或C)。
(4) A溶液的pH大于7,用离子方程式表示原因______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列微粒中中心原子的杂化方式和微粒的立体构型均正确的是( )
A.![]() :sp2、平面三角形B.
:sp2、平面三角形B.![]() :sp3、三角锥形
:sp3、三角锥形
C.C2H4:sp 、平面形D.![]() :sp2、V形
:sp2、V形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有五种元素X、Y、Z、Q、T。X元素为主族元素,X原子的M层上有两个未成对电子且无空轨道;Y原子的价电子排布式为3d64s2;Z原子的![]() 电子层的p能级上有一个空轨道;Q原子的L电子层的p能级上只有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述不正确的是( )
电子层的p能级上有一个空轨道;Q原子的L电子层的p能级上只有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述不正确的是( )
A.元素Y和Q可形成化合物Y2Q3
B.X与![]() 的最高价氧化物对应的水化物,前者的酸性比后者强
的最高价氧化物对应的水化物,前者的酸性比后者强
C.X和Q结合生成的化合物为离子化合物
D.ZQ2是由极性键构成的非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为一恒压容器 。恒温下,将
。恒温下,将![]() 和
和![]() 混合后由
混合后由![]() 口快速充入容器,封闭
口快速充入容器,封闭![]() ,反应N2(g)+3H2(g)
,反应N2(g)+3H2(g)![]() 2NH3(g)在
2NH3(g)在![]() 时刻达到平衡,
时刻达到平衡,![]() 时刻再从
时刻再从![]() 口快速充入一定量
口快速充入一定量![]() ,封闭
,封闭![]() ,
,![]() 时刻重新达平衡至
时刻重新达平衡至![]() 时刻。在
时刻。在![]() 时间内混合气体中
时间内混合气体中![]() 的体积分数(纵坐标)随时间(横坐标)变化的曲线正确的是
的体积分数(纵坐标)随时间(横坐标)变化的曲线正确的是
A. B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO![]()
B.甲基橙呈红色的溶液:NH![]() 、Ba2+、AlO
、Ba2+、AlO![]() 、Cl-
、Cl-
C.与铝反应产生大量氢气的溶液:Na+、K+、CO![]() 、Cl-
、Cl-
D.pH=12的溶液:K+、Na+、CH3COO-、Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.反应热就是反应中放出的能量
B.在任何条件下,化学反应的焓变都等于化学反应的反应热
C.由![]() (s,石墨)═
(s,石墨)═![]() (s,金刚石)
(s,金刚石) ![]() 可知,金刚石比石墨稳定
可知,金刚石比石墨稳定
D.化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com