
����Ŀ��X��Y��W��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ��������������ͼ��ʾ����֪X��һ�ֺ��ص�������Ϊ18��������Ϊ10��Y��Neԭ�ӵĺ�������������1��W�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ķǽ�������ͬ��������Ԫ������ǿ�� 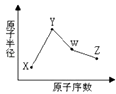
��1��Wλ��Ԫ�����ڱ��е����ڵ��壮����X�������ӵĽṹʾ��ͼ ��
��2��Z���⻯����廯����ȣ����ȶ�������д��ѧʽ����Z���⻯�����������ȣ��е�ϸߵ�����д��ѧʽ����
��3��Y�Ľ�������Mg�Ľ�������ȣ���д��ѧʽ���Ľ�����ǿ������ʵ��֤�����ǽ����Ե����ǿ���� ��
��4��д��Y������������Ӧ��ˮ������Z������������Ӧ��ˮ�������Ӧ�Ļ�ѧ��Ӧ����ʽ�� ��
���𰸡�
��1������IVA��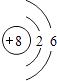
��2��HCl��HF
��3��Na��Na����ˮ���ҷ�Ӧ����Mg����ˮ��Ӧ����
��4��NaOH+HClO4=NaClO4+H2O
���������⣺X��Y��W��Z�����ֳ����Ķ�����Ԫ�أ���֪X��һ�ֺ��ص�������Ϊ18��������Ϊ10����XԪ��ԭ�ӵ�������Ϊ18��10=8����XΪ��Ԫ�أ�Y��Neԭ�ӵĺ�����������1��XΪNa��F��Xԭ�Ӱ뾶������ԭ�ӣ���XΪNaԪ�أ�W�ĵ�����һ�ֳ����İ뵼����ϣ�ԭ����������NaԪ�أ���WΪSiԪ�أ�Z���������ӵ�������ͬ��������Ԫ�������ԭ����������Si����ZΪClԪ�أ���1��WΪSi��ԭ�Ӻ��������Ϊ14����3�����Ӳ㣬����������Ϊ4���������ڱ��е�������IVA�壬XΪO�������ӵĽṹʾ��ͼΪ�� ���Դ��ǣ�����IVA��  ����2��ZΪClԪ�أ�����Ԫ�صķǽ�����Cl��Br�����⻯���ȶ���HCl��HBr�����ȶ�����HCl��������HF����֮���������������˷���֮������������������ʵ��۷е�ϸߵ���HF�����Դ��ǣ�HCl��HF����3��ͬ������ԭ����������ԭ�Ӱ뾶��С��ԭ��ʧȥ���ӵ�����������Ԫ�صĽ��������������Խ�����Na��Mg��Ԫ�صĽ�����Խǿ���䵥����ˮ�����û���������Խ���ף����Կ���ͨ��Na����ˮ���ҷ�Ӧ����Mg����ˮ��Ӧ����֤��Ԫ�صĽ�����Na��Mg�����Դ��ǣ�Na��Na����ˮ���ҷ�Ӧ����Mg����ˮ��Ӧ��������4��Y������������Ӧ��ˮ����NaOH��ǿ�Z������������Ӧ��ˮ����HClO4��һԪǿ�ᣬ���߷�������кͷ�Ӧ�������������ƺ�ˮ��������Ӧ�Ļ�ѧ��Ӧ����ʽ��NaOH+HClO4=NaClO4+H2O��
����2��ZΪClԪ�أ�����Ԫ�صķǽ�����Cl��Br�����⻯���ȶ���HCl��HBr�����ȶ�����HCl��������HF����֮���������������˷���֮������������������ʵ��۷е�ϸߵ���HF�����Դ��ǣ�HCl��HF����3��ͬ������ԭ����������ԭ�Ӱ뾶��С��ԭ��ʧȥ���ӵ�����������Ԫ�صĽ��������������Խ�����Na��Mg��Ԫ�صĽ�����Խǿ���䵥����ˮ�����û���������Խ���ף����Կ���ͨ��Na����ˮ���ҷ�Ӧ����Mg����ˮ��Ӧ����֤��Ԫ�صĽ�����Na��Mg�����Դ��ǣ�Na��Na����ˮ���ҷ�Ӧ����Mg����ˮ��Ӧ��������4��Y������������Ӧ��ˮ����NaOH��ǿ�Z������������Ӧ��ˮ����HClO4��һԪǿ�ᣬ���߷�������кͷ�Ӧ�������������ƺ�ˮ��������Ӧ�Ļ�ѧ��Ӧ����ʽ��NaOH+HClO4=NaClO4+H2O��
���Դ��ǣ�NaOH+HClO4=NaClO4+H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڳ����£�pH=9��NaOH��Һ��CH3COONa������Һ�У�������ˮ���������OH������Ũ�ȷֱ�Ϊa��b����a��b�Ĺ�ϵΪ�� ��
A.a��b
B.a=10��4b
C.b=10��4a
D.a=b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. ʵ����Ӧ���Ʊ�����ú����
B. ��Һ©��������ƿ��ʹ��ǰ��Ҫ��©
C. ���þƾ�����CCl4��ȡ��ˮ�еĵⵥ��
D. ����þʧ����ˮ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ӽ��ܵ�������ˮ�⣬������ǿ����Һ��Ӧ���ǣ�������
A.CH3COO��
B.HSO4��
C.HSO3��
D.CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ�û���ʵ�뽺�������û�й�ϵ���ǣ� ��
A. ��������������ˮ
B. ��ʯ�����±���ƶ���
C. ��CuSO4��Һ����μ����ռ���Һ������ɫ����
D. ���ֵ�Ͳ����ҹ���л����һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ĸ��Թ��У���������ֽ���������ķ�Ӧ���������ǣ�������
�Թ� | �¶� | ����������ҺŨ�� | ���� |
A | ���� | 3% | ���� |
B | ˮԡ���� | 3% | ���� |
C | ˮԡ���� | 6% | MnO2 |
D | ���� | 6% | ���� |
A.A
B.B
C.C
D.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪: A��B��C��D��E��F��G ��ԭ��������������Ķ���������Ԫ�أ�A��ԭ�Ӻ��������ӣ�B��F ��Ԫ�����ڱ��е����λ����ͼ��B ��D ���γ�������ɫ���壬D �ǵؿ��к�������Ԫ�أ�E�ǵؿ��к������Ľ���Ԫ����

��ش���������:
��1��BF2 �ĽṹʽΪ:_____________��
��2��D��F�ļ��⻯���зе�ϸߵ���:________��(�ѧʽ)
��3��ʵ������ȡG2��������ӷ���ʽΪ:____________________��
��4�������ӹ�ҵ�У�C �������̬�ջ����ˮ��Һ������ʴ��H2O2 �����������������Ӧ�IJ��� ����Ⱦ�������仯ѧ����ʽΪ:___________________��
��5��FD2 ����ͨ��BaCl2 ��C������������Ӧ��ˮ����Ļ����Һ�У����ɰ�ɫ��������ɫ���壬 �йط�Ӧ�����ӷ���ʽΪ_____________________��
��6�����ʹ��B2A8C2 ��ȼ�ϣ�N2O4Ϊ��������ȼ�շų��ľ������ܰѻ������̫�գ����Ҳ������� ����Ⱦ�����壬�仯ѧ����ʽΪ:_________________��
��7������Ԫ���������Q: CA4E(FD4)2����ʢ��20 mL 0.5 mol/L Q��Һ���ձ��м���12 mL2.0 mo/LBa(OH)2��Һ����ַ�Ӧ����Һ�в������������ʵ���Ϊ:__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д����ȷ����
A. ������Na2SiO3��Һ���: SiO32-+2H+=H2SiO3��
B. Ũ����Ͷ������̹�����ȡCl2: MnO2+4H++2Cl- ![]() Mn2++Cl2��+2H2O
Mn2++Cl2��+2H2O
C. NO2ͨ��ˮ��: H2O+3NO2=2H++2NO3-+NO
D. �����ʯ��ˮ��ͨ�˹���SO2: SO2+Ca2++2OH-=CaSO4��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧһ������H++OH��=H2O��ʾ�Ļ�ѧ����ʽ�У� ��
A. ����������Һ����ᷴӦ B. ����������ϡ���ᷴӦ
C. ����������ϡ���ᷴӦ D. ����������ϡ���ᷴӦ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com