
| A. |
| B. |
| C. |
| D. |
|
分析 根据元素周期表的结构:相邻两个周期同主族元素的原子序数相差2、8、18、32,以此判断同族中位置关系;同周期元素根据原子序数判断位置关系,据此来分析,注意第三列镧系、锕系,长周期第ⅡA族、第ⅢA族之间有10个空列为7个副族和1个Ⅷ族.
解答 解:A.4和5,12和13间有10个空列为7个副族和1个Ⅷ族,且与5号同主族相邻的下一周期原子序数为13,与6号同主族相邻的下一周期原子序数为14,故A错误;
B.最前列为ⅥA族,最小行为16、17、18,最后列为零族,第一、三周期的原子序数为2、18,符合位置关系,故B正确;
C.1号和11号元素之间相隔一个周期,第一列应为1、3、11、19,2号元素与1号元素之间相隔16列,故C错误;
D.10号元素与4号元素处于同一周期,故D错误.
故选:B.
点评 考查运用原子序数推导元素在周期表中的位置关系,难度中等,关键清楚元素周期表的结构.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂、蛋白质均为高分子化合物 | |
| B. | 苯、邻二甲苯互为同系物 | |
| C. | 棉、麻、羊毛及合成纤维统称为化学纤维 | |
| D. | 合成聚乙烯与合成酚醛树脂的反应类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,7.8g固体Na2O2中,含有的阴阳离子总数为0.4NA | |
| B. | 4℃时,18g 2H216O中含有共用电子对数为2NA | |
| C. | 1 mol N5+含有的电子数为34NA | |
| D. | 用金属铁、Cu片、稀硫酸组成原电池,当金属铁质量减轻5.6g时,流过外电路的电子为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
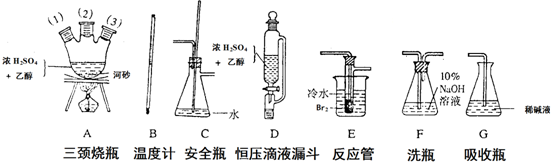
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2O为三角形分子 | |
| B. | N2O与CO2均不含非极性键 | |
| C. | N2O的电子式可表示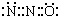 | |
| D. | N2O与SiO2为等电子体、具有相似的结构和相似性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
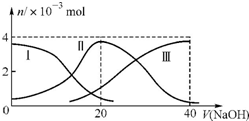 常温下,向20mL0.2mol/L H2C2O4溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化曲线如图所示,[已知CaC2O4难溶于水].根据图示判断,下列说法不正确的是( )
常温下,向20mL0.2mol/L H2C2O4溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化曲线如图所示,[已知CaC2O4难溶于水].根据图示判断,下列说法不正确的是( )| A. | 曲线Ⅱ代表的粒子是HC2O4- | |
| B. | 当V(NaOH)=20ml时,溶液中离子浓度的大小关系为:c(Na+)>c(HC2O4-)>c(C2O42-)>c(H+)>c(OH-) | |
| C. | NaH C2O4溶液中:c(OH-)+c(C2O42-)=c(H+)+c(H2C2O4) | |
| D. | 向NaHC2O4溶液中逐渐加入CaCl2粉末并充分搅拌,溶液PH可能逐渐减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com