
【题目】一定温度下,向容积为2 L的密闭容器中充入一定量的气体A和气体B,发生反应: 2A(g)+B(g) ![]() 2C(g),反应过程中测定部分数据见下表(表中t1<t2),下列说法正确的是
2C(g),反应过程中测定部分数据见下表(表中t1<t2),下列说法正确的是
反应时间/min | n(A)/mol | n(B)/mol |
0 | 0.10 | 0.060 |
t1 | 0.012 | |
t2 | 0.016 |
A. 在0~t1 min内的平均反应速率为v(C)=0.088/t1 molL-1min-1
B. 其他条件不变,起始时向容器中充入0.10 mol C和0.010 mol B,平衡时n(A)=0.012 mol
C. 保持其他条件不变,升高温度,平衡时c(A)=0.0070 molL-1,则反应的ΔH>0
D. 相同温度下,起始时向容器中充入0.15mol A和0.090mol B,平衡时A转化率大于88%
【答案】BD
【解析】
经分析,t1时,n(B)=0.016mol,则t1时该反应已经达到平衡状态,故t2时,n(A)=0.012mol,由此作答。
A. 在0~t1 min内的平均反应速率为v(C)=0.088/2t1 molL-1min-1=0.044/t1 molL-1min1,A错误;
B.根据等效平衡,起始充入0.10mol C和0.010mol ,相当于起始充入了0.10mol A和0.060mol B,所以平衡时n(A)=0.012mol,B正确;
C.保持其他条件不变,升高温度,平衡时c(A)减小,该反应为放热反应,则反应的ΔH<0;C错误;
D. 在原平衡下,参加反应的A的物质的量为0.088mol,则A的转化率为88%,在新的反应体系中,A、B的物质的量增加了,相当于增大了压强,平衡向正方反应方向移动,所以该体系中A的转化率大于88%,D正确;
故合理选项为BD。


科目:高中化学 来源: 题型:
【题目】由硫铁矿“烧渣”(主要成分:Fe3O4、Fe2O3和FeO)制备绿矾(FeSO4·7H2O))的流程如图:

已知:FeS2(S的化合价为-1)难溶于水。
(1)①中加入的酸为___,滤渣2的主要成分是___。
(2)①中生成Fe3+的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O、___。
(3)检验②中Fe3+已经完全转化成Fe2+的实验方法:取适量溶液2,___。
(4)通过③得到绿矾晶体的实验操作:加热浓缩、冷却结晶、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如下。下列说法不正确的是( )
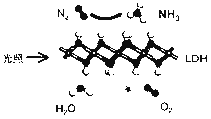
A. 该过程将太阳能转化成为化学能 B. 该过程中,涉及极性键与非极性键的断裂与生成
C. 氧化产物与还原产物的物质的量之比为3∶4 D. 该反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
(1)C在元素周期表中的位置为______,G的原子结构示意图是____。
(2)D与E按原子个数比1:1形成化合物甲,其电子式为____,所含化学键类型为____。向甲中滴加足量水时发生反应的化学方程式是______。
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序是_____。(用离子符号表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各图像的解释或结论正确的是

A. 图①可表示用NaOH溶液滴定等浓度醋酸溶液,溶液导电性随NaOH的体积变化
B. 图②可表示25℃时,0.10 molL-1盐酸滴定20.00mL0.10 molL-1NaOH溶液的滴定曲线
C. 图③表示水溶液中c(H+)与c(OH-)的变化关系,则水的电离程度(![]() ):
):![]() ;水的离子积:KW(d)=KW(b)
;水的离子积:KW(d)=KW(b)
D. 图④表示合成氨N2(g)+3H2(g) ![]() 2NH3(g) △H<0的平衡常数与温度和压强的关系
2NH3(g) △H<0的平衡常数与温度和压强的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列四组实验,现象和结论均正确的是( )
操作 | 现象 | 结论 | |
A | 滴加稀NaOH溶液,将红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH |
B | 将SO2通入Ba(NO3)2溶液中 | 出现白色沉淀 | 沉淀为BaSO3 |
C | 在Na2S溶液中滴加新制氯水 | 产生浅黄色沉淀 | 非金属性:C1>S |
D | 将稀硝酸加入过量铁粉中,充分反应后,滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化成Fe3+ |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将质量为mg的铜屑完全溶于适量浓硝酸中,反应后得到NO2、NO的混合气体,将所得气体通入300mL2molL-1NaOH溶液中,恰好完全反应,生成含NaNO3和NaNO2的盐溶液,其中NaNO3的物质的量为0.2mol,则m的值为( )
A.12.8B.19.2C.25.6D.51.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A. 14 g乙烯和丙烯混合气体中的氢原子数为2NA
B. 1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C. 1 mol Fe溶于过量硝酸,电子转移数为2NA
D. 标准状况下,2.24 L CCl4含有的共价键数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题。
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧
⑧![]()
(1)只含有离子键的是______(填序号,下同)
(2)含有共价键的离子化合物是______,其中含有非极性共价键的物质的电子式为______。
(3)属于共价化合物的是______。
(4)熔融状态下能导电的化合物是______。
(5)熔融状态下和固态时都能导电的物质是______。
(6)用电子式表示![]() 的形成过程:______。
的形成过程:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com