
下列事实中,不能用平衡移动原理解释的是
A.开启啤酒瓶后,瓶中马上泛起大量泡沫
B.对CO(g)+NO2(g) CO2(g)+NO(g)平衡体系增大压强可使其颜色变深
CO2(g)+NO(g)平衡体系增大压强可使其颜色变深
C.常温下,将1mLpH=3的醋酸溶液加水稀释到100mL,测得其pH<5
D.实验室中常用排饱和食盐水的方法收集氯气
科目:高中化学 来源:2016届河北省高三上一轮收官考试理综化学试卷(解析版) 题型:实验题
高锰酸钾(KMnO4)是常用的氧化剂,工业上以软锰矿(主要成分是MnO2)为,原料制备高锰酸钾晶体。中间产物为锰酸钾(K2MnO4)下图1是实验室模拟制备的操作流程:
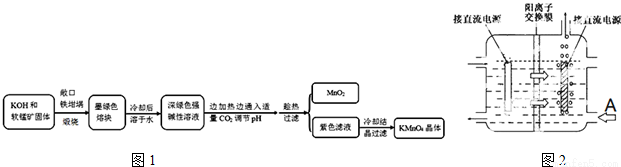
相关资料:
①物质溶解度
物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
②锰酸钾[K2MnO4]外观性状:墨绿色结晶.其水溶液呈深绿色,这是锰酸根(MnO42-)的特征颜色.
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42-会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是______________;实验中用 铁坩埚煅烧暴露在空气中的固体混合物发生反应的化学方程式为______________。
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式______________;其中氧化还原反应中氧化剂和还原剂的质量比为________。
(3)由于CO2的通人量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中_______,得到的产品纯度更高.
A.醋酸 B.浓盐酸 C.稀硫酸
(4)工业上一般采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式______________;传统工艺采用无膜电解法由于副反应发生,Mn元素利用率和电流效率都会偏低.有同学联想到离子交换膜法电解饱和食盐水提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图2).图中A口加入的溶液最好为_________;使用阳离子交换膜可以提高Mn元素利用率的原因为______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上期中测试化学试卷(解析版) 题型:选择题
下列各组物质中,按化合物、单质、混合物顺序排列的一组是( )
A.烧碱、液态氧、碘酒 B.生石灰、白磷、熟石灰
C.干冰、铁、氯化氢 D.空气、氮气、明矾
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上二调考试化学试卷(解析版) 题型:填空题
(1)将0.2mol/L HA 溶液与 0.1mol/L NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A?),则(用“>”、“<”或“=”填写下列空白):①混合溶液中c(A?)______c(HA);②混合溶液中c(HA)+c(A?)______0.1mol?L?1;
(2)常温时,取0.1mol•L-1 HX溶液与0.1mol•L-1 NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
①混合溶液中由水电离出的c(OH-)与0.1mol•L-1 NaOH溶液中由水电离出的c(OH-)之比为______.
②已知NH4X溶液是中性,又知将HX溶液加入到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH______7(选填“>”、“<”或“=”).
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上二调考试化学试卷(解析版) 题型:选择题
在由水电离产生的H+浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是
①K+、Cl-、NO3-、S2- ②K+、Fe3+、I-、SO42-
③Na+、Cl-、NO3-、SO42- ④Na+、Ca2+、Cl-、HCO3- ⑤K+、Ba2+、Cl-、NO3-
A.①③ B.③⑤ C.③④ D.②⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上期中(文)化学试卷(解析版) 题型:选择题
下列反应的离子方程式中,书写错误的是
A.硫酸氢钠溶液与氢氧化钠溶液反应:H++OH-=H2O
B.新制氯水与溴化钾溶液反应:Cl2+2Br-=2Cl-+Br2
C.碳酸钙与稀盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑
D.铝与烧碱溶液反应:2Al+2H2O+2OH-=AlO2-+2H2↑
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期期中考试化学试卷(解析版) 题型:填空题
(Ⅰ)浓硝酸与浓盐酸混合过程中会产生少量的黄绿色气体单质X、化合物M和无色液体,化合物M中所有原子均达到8电子的稳定结构。2mol M加热分解生成1mol氧化产物X和2mol无色气体Y,Y遇到空气呈现红棕色。
(1)镁与气体X反应产物的电子式 。
(2)浓硝酸与浓盐酸反应的化学方程式为 。
(3)化合物M水解生成两种酸,为非氧化还原反应,该反应的化学方程式为 。
(Ⅱ)石油铁储罐久置未清洗易引发火灾,经分析研究,事故是由罐体内壁附着的氧化物甲与溶于石油中的气态氢化物乙按1︰3反应生成的物质丙自燃引起的。某研究小组将一定量的丙粉末投入足量的浓盐酸中发生反应,得到4.8g淡黄色固体和气体乙,乙在标准状况下的密度为1.52g·L-1。过滤后向滤液(假设乙全部逸出)中加入足量的NaOH溶液,先出现白色沉淀,最终转变为红褐色沉淀,过滤、洗涤、灼烧后的固体质量为24g。已知气体乙可溶于水。请回答下列问题:
(4)甲的化学式为 。
(5)丙在盐酸中反应的化学方程式为 。
(6)丙与盐酸反应后的滤液暴露在空气中一段时间颜色加深,其原因是(用离子方程式表示) 。
(7)为消除石油铁储罐的火灾隐患,下列措施可行的是(填编号) 。
A.石油入罐前脱硫 B.定期用酸清洗罐体
C.罐体内壁涂刷油漆 D.罐体中充入氮气
查看答案和解析>>
科目:高中化学 来源:2016届浙江绍兴市高三上学期期中考试化学试卷(解析版) 题型:简答题
将总物质的量为4mol的Na2O2和Al2(SO4)3混合物投入足量水中,充分反应后生成ymol沉淀(y≠0)。若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值与y=f(x)关系式填写在表内(可填满,也可不填满或补充),并在右图中画出函数图象。

x值 | y=f(x) |
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.等物质的量浓度的FeBr2和CuCl2的混合液用惰性电极电解最初发生:Cu2++2Br-=Cu↓+Br2
B.H218O中投入Na2O2:2H218O+2Na2O2=4Na++4OH-+即O2↑
C.向明矾溶液中逐滴加入Ba(OH)2溶液到SO42-恰好沉淀完全:
2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
D.Fe(NO3)3的酸性溶液中通入足量硫化氢:2Fe3++H2S=2Fe2++S↓+2H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com